已知醋酸是日常生活中常见的弱酸.(1)用pH试纸测定醋酸pH的操作是 .(2)常温下在 pH =5的醋酸稀溶液中.醋酸电离出的c(H+)的精确值是 mol?L
糖醋排骨的糖醋比例一般是1:1:醋的酸味能中和糖的甜,口感酸甜适中。 #生活常识# #烹饪秘籍#
(14分)已知醋酸是日常生活中常见的弱酸。
(1)用pH试纸测定醋酸pH的操作是___________。
(2)常温下在 pH =5的醋酸稀溶液中,醋酸电离出的c(H+)的精确值是______ mol?L—1。
(3)用0.1000 mol?L—1NaOH溶液滴定20.00mL某浓度的CH3COOH溶液,部分操作如下:
①取一支用蒸馏水洗净的碱式滴定管,加入标准氢氧化钠溶液,记录初始读数
②用酸式滴定管放出一定量待测液,置于用蒸馏水洗净的锥形瓶中,加入2滴甲基橙
③滴定时,边滴加边振荡,同时注视滴定管内液面的变化
请选出上述实验过程中的错误之处
(填序号)。上述实验与一定物质的量浓度溶液配制实验中用到的相同仪器___________________。
(4)某次滴定前滴定管液面如图所示,读数为________mL。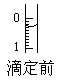

(5)根据正确实验结果所绘制的滴定曲线如上图所示,其中点①所示溶液中c(CH3COO-)=1.7c(CH3COOH),点③所示溶液中c(CH3COO-)+c(CH3COOH)=c(Na+)。计算醋酸的电离平衡常数___________,CH3COOH的物质的量浓度为__________ mol?L—1。
(14分)(1) 用镊子夹取一小块试纸放在干燥洁净的表面皿或玻璃片上,用玻璃棒蘸取待测液点在试纸的中部,观察颜色变化,与标准比色卡比对读数(2分)
(2)10—5—10—9(2分)
(3) ①②③(2分) 烧杯(或烧杯和胶头滴管)(2分)
(4)0.30(2分)
(5)1.7×10—5 mol?L—1(2分) 0.1007(2分)
(1)考查常见的基本实验操作。测量溶液的pH值的正确方法是用镊子夹取一小块试纸放在干燥洁净的表面皿或玻璃片上,用玻璃棒蘸取待测液点在试纸的中部,观察颜色变化,与标准比色卡比对读数。
(2)常温下在 pH =5的醋酸稀溶液中,氢离子浓度是10—5 mol/L。由于水还存在电离平衡,所以醋酸电离出的c(H+)的精确值是10—5 mol/L—10—9 mol/L。
(3)滴定管在装入标准液之前需要润洗,①不正确;醋酸是弱酸,所以氢氧化钠滴定醋酸时,应该用酚酞试液作指示剂,②不正确;滴定时,边滴加边振荡,同时注视锥形瓶内溶液颜色的变化,③不正确,所以答案选①②③。配制一定物质的量浓度溶液和中和滴定值都需要烧杯。
(4)滴定管的能精确到0.1ml,读数到0.01ml。又因为滴定管的刻度自上而下时逐渐增大的,所以根据液面的位置可知,正确的读数是0.30ml。
(5)①点溶液中氢离子浓度是10—5 mol/L,所以醋酸的电离平衡常数是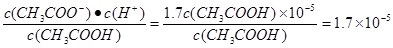 。点③所示溶液中c(CH3COO-)+c(CH3COOH)=c(Na+),所以恰好满足物料守恒,即点③处溶液中溶质是醋酸钠,这说明二者恰好反应,所以根据消耗氢氧化钠溶液的条件是20.14ml可知,醋酸的浓度是0.1000mol/L×20.14÷20=0.1007mol/L。
。点③所示溶液中c(CH3COO-)+c(CH3COOH)=c(Na+),所以恰好满足物料守恒,即点③处溶液中溶质是醋酸钠,这说明二者恰好反应,所以根据消耗氢氧化钠溶液的条件是20.14ml可知,醋酸的浓度是0.1000mol/L×20.14÷20=0.1007mol/L。
练习册系列答案
相关习题
科目:高中化学来源:不详题型:单选题
在室温下,等体积的酸和碱的溶液混合后,pH一定少于7的是
A.pH=3的醋酸跟pH=11的氢氧化钠溶液B.pH=3的盐酸跟pH=11的氨水C.pH=3硫酸跟pH=11的氢氧化钠溶液D.pH=3的HNO3跟pH=11的KOH溶液查看答案和解析>>
科目:高中化学来源:不详题型:单选题
向纯水中加入少量NaHSO4,在温度不变时,溶液中( )
A.c(H+)/c(OH-)增大B.c(H+)减小C.水中c(H+)与c(OH-)的乘积增大D.c(OH-)增大查看答案和解析>>
科目:高中化学来源:不详题型:填空题
(7分)用稀盐酸和氢氧化钡溶液进行酸碱中和反应实验,该反应过程中溶液酸碱度变化及相关数据如右图所示。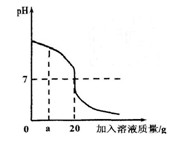
(1)根据此变化曲线,你认为实验操作是将
滴加到另一种溶液中。
(2)当加入溶液质量是a g时,溶液中溶质是
(写化学式)。
(3)若用pH试纸测定溶液的酸碱度,请写出测定方法:
。
(4)当pH=7时,测得生成氯化钡的物质的量为0.05mol,求盐酸中溶质的质量分数?
查看答案和解析>>
科目:高中化学来源:不详题型:单选题
下列有关反应热的说法中正确的是( )
A.一个化学反应是否能在常温下发生,与该反应的△H值的大小没有必然联系B.中和热△H=-57.3kJ·mol-1,所以1.00L 1.00mol·L-1H2SO4与稀的NaOH溶液恰好完全反应放出57.3kJ的热量C.用等体积的0.50mol·L-1盐酸、0.55mol·L-1NaOH溶液进行中和热测定的实验,会使测得的值偏大D.在101kPa时,1molCH4完全燃烧生成CO2和水蒸气放出的热量是CH4的燃烧热查看答案和解析>>
科目:高中化学来源:不详题型:实验题
50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题: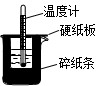
(1)从实验装置看,图中尚缺少的一种玻璃用品是_______________。
(2)烧杯间填满碎纸条的作用是_________________________。
(3)实验中改用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比较,所放出的热量__________(填“相等”或“不相等”),中和热__________(填“相等”或“不相等”),理由是__________________________________。
(4)用50mL0.50mol/L的醋酸代替盐酸溶液进行上述实验,测得中和热的数值与57.3kJ/mol相比较会____________。(填“偏大”、“偏小”或“无影响”)。
(5)完整地做一次这样的实验,需测定______次温度。
(6)大烧杯上如不盖硬纸板,求得的中和热数值
(填“偏大”、“偏小”或“无影响”)
查看答案和解析>>
科目:高中化学来源:不详题型:单选题
科学家预测“氢能”将是21世纪最理想的新能源。化学家提出“硫-碘热循环法”制氢气,总反应方程式为:,其循环过程分三步进行:
(a) SO2+I2+2H2O=2HI+H2SO4 (b) 2HI=H2+I2 (c) 2H2SO4=2SO2+O2+2H2O。
下列分析不合理的是 ( )
查看答案和解析>>
科目:高中化学来源:不详题型:单选题
常温下,下列溶液中的微粒浓度关系正确的是
A.新制氯水中加入固体NaOH:c(Na+)=c(Cl-)+c(ClO-)+c(OH-) B.pH=8.3的NaHCO3溶液:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) C.pH=11的氨水与pH=3的盐酸等体积混合:c(Cl-)=c(NH4+) >c(OH-)=c(H+)D.0.2mol·L-1CH3COOH溶液与0.1mol·L-1NaOH溶液等体积混合:2c(H+)-2c(OH-)=C(CH3COO-)-C(CH3COOH)查看答案和解析>>
科目:高中化学来源:不详题型:单选题
下列燃烧反应的反应热是燃烧热的是( )
A.H2(g)+O2(g)===H2O(g) ΔH1B.C(s)+O2(g)===CO(g) ΔH2C.S(s)+O2(g)===SO2(g) ΔH3D.H2S(g)+O2(g)===S(s)+H2O(l) ΔH4查看答案和解析>>
网址:已知醋酸是日常生活中常见的弱酸.(1)用pH试纸测定醋酸pH的操作是 .(2)常温下在 pH =5的醋酸稀溶液中.醋酸电离出的c(H+)的精确值是 mol?L https://www.yuejiaxmz.com/news/view/352252
相关内容
Ⅰ.醋酸(已知:25℃,Ka(CH3COOH)=1.69×10-5)是日常生活中最常见的调味剂和重要的化工原料。下列实验方案能说明醋酸是弱酸的是(1)已知25℃时有关弱酸的电离平衡常数:弱酸化学式HSCNCH3COOHHCNH2CO3电离平衡常数1.3×10
碱性最强的是( )A. 牙膏pH=9 B. 食盐水pH=7 C. 白醋pH=3 D. 洗洁精pH=11 D [解析]白醋的pH=3.显酸性,食盐水pH=7.显中性,洗洁精.牙膏等物质的pH大于7.显碱性.洗洁精的pH最大.碱性最强.故选D. 题目和参考答案——青夏教育精英家教网——
醋酸钠的用途是什么?
用简短的文字和方程式解答下列问题:(1)Na2CO3溶液可做洗涤剂去除油污.而且热的溶液去污效果更好.其原因是 .(2)实验室有两瓶失去标签且pH=3的溶液.已知它们是稀盐酸和醋酸.请写出区别它们的一种方法: . 题目和参考答案——青夏教育精英家教网——
小军同学在学完“酸的化学性质 后.邀请你与他讨论“食醋在厨房中的妙用 :(1)复习酸的化学性质①酸与指示剂作用酸溶液能使紫色石蕊溶液变红色酸溶液不能使无色酚酞溶液变色②酸与活泼金属作用Fe+2HCl=FeCl2+H2↑Fe+H2SO4=FeSO4+H2↑③酸与某些金属氧化物作用Fe2O3+HCl=FeCl3+H2O
人类的日常生活离不开酸.碱.盐三类物质.请回答下列问题:(1)山药中含有碱性皂角素.皮肤沾上会奇痒难忍.你认为可涂厨房中的 来止痒,(2)①酸奶,②肥皂水,③食盐水,是生活中常见的三种物质.酸奶能使紫色石蕊试液变红.肥皂水显碱性.食盐水的pH=7.它们的pH由小到大的顺序为 ,(3)在树木上涂刷含有硫磺粉的石灰浆.作用是 .(4)服用含有氢氧化铝的药物可以治疗胃酸 题目和参考答案——青夏教育精英家教网——
生活中的常见物品及其pH如下,其中碱性最强的是A.肥皂水pH=10B.食醋pH=2.9C.纯牛奶pH=6.5D.炉具清洁剂pH=12.4
已知生活中厕所清洁剂的pH=1.厨房的清洁剂的pH=12.下列关于两者的说法不正确的是( )A. 厕所清洁剂加水稀释.溶液pH升高 B. 厨房清洁剂可能含有NaOHC. 混合使用能提高两者的清洁效果 D. 厕所清洁剂可能使铁制下水道腐蚀 C [解析]溶液的pH小于7.溶液呈酸性.pH越小.酸性越强,溶液的pH大于7.溶液呈碱性.pH越大碱性越强,pH等于7.溶液 题目和参考答案——青夏教育精英家教网——
下列是生活中常见物质的pH.其中碱性最强的是A.厕所清洁剂pH=1 B.食醋pH=3 C.肥皂水pH=10 D.厨房洗涤剂pH=12 题目和参考答案——青夏教育精英家教网——

