低碳经济呼唤新能源和清洁环保能源.煤化工中常需研究不同温度下的平衡常数.投料比及热值等问题.已知:CO(g) + H2O(g)H2(g) + CO2(g) △H= a kJ·mol
度假村G:在山区,有徒步和滑雪设施,冬季是热门选择。 #生活知识# #旅行生活# #度假村推荐#
相关习题
0 55830 55838 55844 55848 55854 55856 55860 55866 55868 55874 55880 55884 55886 55890 55896 55898 55904 55908 55910 55914 55916 55920 55922 55924 55925 55926 55928 55929 55930 55932 55934 55938 55940 55944 55946 55950 55956 55958 55964 55968 55970 55974 55980 55986 55988 55994 55998 56000 56006 56010 56016 56024 203614
科目:来源:2013届湖南省五市十校高三第一次联合检测化学试卷(带解析)题型:填空题
( 10分)低碳经济呼唤新能源和清洁环保能源。煤化工中常需研究不同温度下的平衡常数、投料比及热值等问题。已知:CO(g) + H2O(g)H2(g) + CO2(g) △H= a kJ·mol-1 的平衡常数随温度的变化如下表:
(1)上述正反应方向是
反应(填“放热”或“吸热”)。
t1℃时物质浓度(mol/L)的变化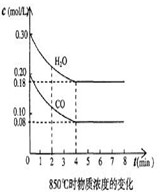
CO
H2O
CO2
H2
0
0.200
0.300
0
0
2
0.138
0.238
0.062
0.062
3
c1
c2
c3
c3
4
c1
c2
c3
c3
5
0.116
0.216
0.084
6
0.096
0.266
0.104
(2) t1℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如上表。①与2min时相比,3min时密闭容器中混合气体的平均摩尔质量
(填增大、减小或不变)。
②表中3 min~4 min之间反应处于
状态;CO的体积分数
16% (填大于、小于或等于)。
③反应在4 min~5 min,平衡向逆方向移动,可能的原因是____(单选),表中5 min~6 min之间数值发生变化,可能的原因是______(单选)。
A.增加水蒸气 B.降低温度 C.使用催化剂 D.增加氢气浓度
(3)若在500℃时进行,若CO、H2O的起始浓度均为0.020mol/L,在该条件下,CO的最大转化率为
。
查看答案和解析>>
科目:来源:2012-2013学年重庆市重庆一中高二上学期期末考试化学试卷(带解析)题型:填空题
(1)80℃时,将0.40 mol的N2O4气体充入2L已经抽空的固定容积的密闭容器中,发生如下反应:N2O4 (g) 2NO2 (g) △H>0,隔一段时间对该容器内的物质进行分析,得到如下数据:
n(mol)
0
20
40
60
80
110
n(N2O4)
0.40
a
0.20
c
d
e
n(NO2)
0.00
0.24
b
0.52
0.60
0.60
①上表中c =___________;e =_____________
②计算20s—40s内用NO2表示的平均反应速率为
mol/(L·s)
③计算在80℃时该反应的平衡常数K=
;
(2)若(1)中反应进行至110s后,保持温度和体积不变,向容器中再加入0.2mol N2O4,此时,平衡朝_______方向移动;建立新平衡后,N2O4的转化率_______75%(填“>、<或=”);
(3)若(1)中反应进行至110s后,保持温度和体积不变,向容器中再加入0.2mol N2O4和0.1mol NO2时,v正________ v逆(填“>、<或=”)
查看答案和解析>>
科目:来源:2012-2013学年重庆市杨家坪中学高二12月月考化学试卷(带解析)题型:填空题
(16分)恒温时,将2molA和2molB气体投入固定容积为2L密闭容器中发生反应: 2A(g) + B(g) xC (g) + D(s) ,10s时,测得A的物质的量为1.7mol,C的反应速率为0.0225mol·L—1·s—1;40s时反应恰好处于平衡状态,此时B的转化率为20%。(1)x = (2)从反应开始到40s达平衡状态,A的平均反应速率为 (3)平衡时容器中B的体积分数为 (4)该温度下此反应的平衡常数表达式为 数值是 (5)下列各项能表示该反应达到平衡状态是
A.消耗A的物质的量与生成D的物质的量之比为2∶1 B.容器中A、B的物质的量 n(A)∶n(B) ="2∶1"
C.气体的平均相对分子质量不再变化 D.压强不再变化 E.气体密度不再变化
(6)在相同温度下,若起始时c(A)="5" mol·L-1,c(B)=6mol·L-1,反应进行一段时间后,测得A的浓度为3mol·L-1,则此时该反应是否达到平衡状态 (填“是”与“否”),此时v(正) v(逆)(填“大于”“小于”或“等于”)。
查看答案和解析>>
科目:来源:2013届黑龙江省哈尔滨九中高三第四次(12月)月考化学试卷(带解析)题型:填空题
(11分)工业制硝酸的主要反应是:4NH3(g)+5O2(g)4NO(g)+6H2O (g) ΔH=" -1025" KJ/mol
(1)一定温度下,现将0.8mol NH3和1.5mol O2充入一恒压密闭容器中,下列示意图正确且能说明反应达到平衡状态的是 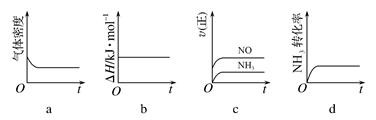
(2)在容积为1L的密闭容器中发生上述反应,容器内部分物质的物质的量浓度如下表:
c(NH3)(mol/L)
C(O2)(mol/L)
C(NO)(mol/L)
起始
0.8
1.5
0
第2min
0.7
a
0.1
第4min
0.4
1.0
0.4
第6min
0.4
1.0
0.4
第8min
1.2
2.5
0.4
①起始时物料比c (O2) : c (NH3)>1.25,其原因是
②反应在第2min到第4min时O2的平均反应速率为
mol·L-1·min-1
③反应在第2min改变了反应条件,改变的条件可能是
(填字母序号)
a.使用催化剂 b.升高温度 c.增大压强 d.增加O2的浓度
④反应在第8min改变的反应条件可能是
,再次达到平衡时,NO的体积分数
(填“增大”、“减小”或“不变”)
(3)室温下,将第一次达到平衡时的混合气体通入水中,然后向该溶液滴加b L氨水后溶液呈中性,则滴加氨水的过程中,溶液中水的电离平衡将
(填“正向”“ 逆向”或“不”)移动,所滴加氨水的浓度为
mol·L-1。(NH3·H2O的电离平衡常数Kb=2×10-5 mol·L-1)
查看答案和解析>>
科目:来源:2013届山东省德州市某中学高三12月月考化学试卷(带解析)题型:填空题
(6分)在容积为10L的密闭容器中,通入40molN2和120molH2,在一定条件下进行反应,2s后达到平衡状态,此时N2的浓度是2mol/L,试求:
(1)用H2的浓度变化表示的2s内的平均反应速率为多少?
(2)N2的转化率为多少?
(3)平衡时NH3的体积分数为多少?(要求有计算过程)
查看答案和解析>>
科目:来源:2013届山东省德州市某中学高三12月月考化学试卷(带解析)题型:填空题
(3分)牙齿的损坏实际是牙釉质[Ca5(PO4)3OH]溶解的结果,在口腔中存在如下平衡:Ca5(PO4)3OH5Ca2+ +3PO43― +OH―当糖附在牙齿上发酵时会产生H+,试运用化学平衡理论说明经常吃糖对牙齿的影响。
查看答案和解析>>
科目:来源:2013届山东省德州市某中学高三12月月考化学试卷(带解析)题型:填空题
查看答案和解析>>
科目:来源:2013届山东省德州市某中学高三12月月考化学试卷(带解析)题型:填空题
(10分)在密闭容器中,通入xmolH2和ymolI2(g),存在H2+I2(g)2HI(g)正反应为放热反应,改变下列条件,反应速率将如何改变(填增大、减小、或不变),平衡将如何改变(填向左、向右或不)
①升高温度,反应速率将 ,平衡将 移动。
②加入催化剂,反应速率将 ,平衡将 移动。
③充入更多的H2,反应速率将 ,平衡将 移动。
④扩大容器的体积,反应速率将 ,平衡将 移动。
⑤容器容积不变,通入氖气,反应速率将 ,平衡将 移动。
查看答案和解析>>
科目:来源:2013届甘肃省甘谷一中高三第五次检测化学试卷(带解析)题型:填空题
已知2X2(g)+Y2(g) = 2Z(g) ΔH=-akJ·mol-1(a>0),在一个容积固定的容器中加入2mol X2和1mol Y2,在500℃时充分反应达平衡后Z的浓度为W mol·L-1,放出热量b kJ。
⑴此反应平衡常数表达式为_________________;若将温度降低到300℃,则反应平衡常数将___________(填增大、减少或不变)。
⑵若原来容器中只加入2mol Z,500℃充分反应达平衡后,吸收热量c kJ,则Z浓度_______Wmol·L—1(填“>”、“<”或“=”),a、b、c之间满足关系___________(用代数式表示)。
⑶能说明反应已达平衡状态的是___________________。
⑷若将上述容器改为恒压容器(反应器开始体积相同),相同温度下起始加入2mol X2和1mol Y2达到平衡后,Y2的转化率将_____(填“变大”、“变小”或“不变”)。
查看答案和解析>>
科目:来源:2013届辽宁省东北育才双语学校高三第五次模拟化学试卷(带解析)题型:填空题
汽车尾气里含有NO气体是由于内燃机燃烧的高温引起氮气和氧气反应所致:
N2(g) + O2(g) 2NO(g) △H > 0
已知该反应在2404℃时,平衡常数K=64×10-4。请回答:
(1)该反应的平衡常数表达式为
(2)该温度下,向2L密闭容器中充入N2和O2各1mol,平衡时,N2的转化率是 %(保留整数)。
(3)该温度下,某时刻测得容器内N2、O2、NO的浓度分别为2.5×10-1mol/L、4.0×10-2mol/L 和3.0×10-3mol/L,此时反应 (填“处于化学平衡状态”、“向正反应方向进行”或“向逆反应方向进行”),理由是 .
(4)将N2、O2的混合气体充入恒温恒容密闭容器中,下列变化趋势正确的是 (填字母序号)。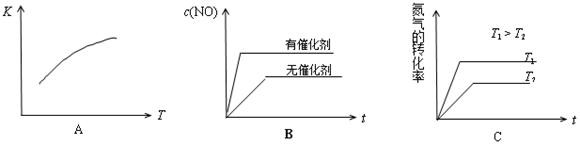
(5)向恒温恒容的密闭容器中充入等物质的量的N2和O2,达到平衡状态后再向其中充入一定量NO,重新达到化学平衡状态。与原平衡状态相比,此时平衡混合气中NO的体积分数 (填“变大、“变小”或“不变)
查看答案和解析>>
网址:低碳经济呼唤新能源和清洁环保能源.煤化工中常需研究不同温度下的平衡常数.投料比及热值等问题.已知:CO(g) + H2O(g)H2(g) + CO2(g) △H= a kJ·mol https://www.yuejiaxmz.com/news/view/219739
相关内容
消除含氮化合物对大气和水体的污染是环境保护的重要研究课题。(1)已知:反应ⅠN2(g)+O2(g)=2NO(g)ΔH=akJ·mol-1反应Ⅱ2NO(g)+O2日常生活、生产中甲烷既是重要的清洁能源也是一种重要的化工原料.(1)如图1是CH4/H2O体系放氢焓变示意图:则CH4(g)+CO2(g)=2CO(g)+2H2(g)△H=
甲醇是人们开发和利用的一种新能源.已知:①2H2(g)+O2(g)═2H2O(l)△H1=
丙烯是重要的有机化工原料,丁烯催化裂解法是一种重要的丙烯生产法,生产过程中会有生成乙烯的副反应发生。反应如下:I主反应,3C4H8(g)=4C3H6(g)△H1
随着化石能源的减少.新能源的开发利用日益迫切.(1)Bunsen热化学循环制氢工艺由下列三个反应组成:SO2(g)+I2(g)+2H2O+H2SO4(l)△H=a kJ?mol
(14分)钢铁生产中的尾气易造成环境污染,清洁生产工艺可消减污染源并充分利用资源。已知:①3Fe2O2(s)+CO(g)2Fe3O2(s)+CO2(g)△H=—47kJ/mol②Fe3O3(s)+3CO(g)2Fe(s)+3CO2(g)△H=—
对大气污染物SO2、NOx进行研究具有重要环保意义。请回答下列问题:(1)为减少SO2的排放,常采取的措施是将煤转化为清洁气体燃料。已知:H2(g)+O2(g)=H2O(g)△H=-241.8kJ·mol-1C
随着环保意识增强.清洁能源越来越受到人们关注.(1)甲烷是一种理想的洁净燃料.已知:CH4(g)+2O2(g)═CO2(g)+2H2O(g),△H=
煤的气化是高效.清洁的利用煤炭的重要途径之一.(1)焦炭与水蒸气反应是将固体煤变为气体燃料的方法.已知:①C(s)+O2 (g)=CO2 (g)△H=
(1)甲烷是一种高效清洁的新能源.0.25mol甲烷完全燃烧生成液态水时.放出222.5kJ热量.则甲烷燃烧热的热化学方为CH4(g)+2O2(g)→CO2(g)+2H2O(l)△H=

