开发使用清洁能源.发展“低碳经济 正成为科学家研究的主要课题.氢气.甲醇是优质的清洁燃料.可制作燃料电池.(1)甲烷水蒸气转化法制H2的主要转化反应如下:CH4(g) + H2O(g) CO(g) + 3H2(g)? △H=+206.2 kJ·mol
燃料电池汽车使用氢气或甲醇等作为燃料,排放物主要为水蒸气。 #生活知识# #科技生活# #科技改变生活# #新能源应用#
开发使用清洁能源,发展“低碳经济”正成为科学家研究的主要课题。氢气、甲醇是优质的清洁燃料,可制作燃料电池。
(1)甲烷水蒸气转化法制H2的主要转化反应如下:
CH4(g) + H2O(g) CO(g) + 3H2(g)? △H=+206.2 kJ·mol-1
CH4(g) + 2H2O(g)CO2(g) + 4H2(g)? △H=+165.0 kJ·mol-1
上述反应所得原料气中的CO能使合成氨的催化剂中毒,必须除去。工业上常采用催化剂存在下CO与水蒸气反应生成易除去的CO2,同时可制得等体积的氢气的方法。此反应称为一氧化碳变换反应,该反应的热化学方程式是??????? 。
(2)生产甲醇的原料CO和H2来源于:CH4(g) + H2O(g) CO(g) + 3H2(g)? ΔH>0
①一定条件下CH4的平衡转化率与温度、压强的关系如图a。则A、B、C三点处对应平衡常数(KA、KB、KC)的大小关系为___________。(填“<”、“>”、“=” );

②100℃时,将1 mol CH4和2 mol H2O通入容积为1 L的定容密封容器中,发生反应,能说明该反应已经达到平衡状态的是__________
a.容器内气体密度恒定??
b.单位时间内消耗0.1 mol CH4同时生成0.3 mol H2
c.容器的压强恒定??????
d.3v正(CH4) = v逆(H2)
(3)25℃时,在20mL0.1mol/L氢氟酸中加入VmL0.1mol/LNaOH溶液,测得混合溶液的pH变化曲线如图所示,下列说法正确的是_____。
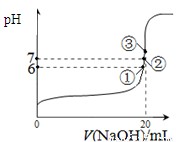
A.pH=3的HF溶液和pH=11的NaF溶液中, 由水电离出的c(H+)相等
B.①点时pH=6,此时溶液中,c(F-)-c(Na+)=9.9×10-7mol/L
C.②点时,溶液中的c(F-)=c(Na+)
D.③点时V=20mL,此时溶液中c(Na+)=0.1mol/L
(4)长期以来,一直认为氟的含氧酸不存在。1971年美国科学家用氟气通过细冰末时获得HFO,其结构式为H—O—F。HFO与水反应得到HF和化合物A,该反应的化学方程式为????????????????????? 。
网址:开发使用清洁能源.发展“低碳经济 正成为科学家研究的主要课题.氢气.甲醇是优质的清洁燃料.可制作燃料电池.(1)甲烷水蒸气转化法制H2的主要转化反应如下:CH4(g) + H2O(g) CO(g) + 3H2(g)? △H=+206.2 kJ·mol https://www.yuejiaxmz.com/news/view/244787
相关内容
丙烯是重要的有机化工原料,丁烯催化裂解法是一种重要的丙烯生产法,生产过程中会有生成乙烯的副反应发生。反应如下:I主反应,3C4H8(g)=4C3H6(g)△H1日常生活、生产中甲烷既是重要的清洁能源也是一种重要的化工原料.(1)如图1是CH4/H2O体系放氢焓变示意图:则CH4(g)+CO2(g)=2CO(g)+2H2(g)△H=
近几年.大气污染越来越严重.雾霾天气对人们的生活.出行.身体健康产生许多不利的影响.汽车尾气是主要的大气污染源.降低汽车尾气危害的方法之一是在排气管上安装催化转化器.发生的反应为:则,△H= kJ(用含a.b.c.d的式子表示).(2)某温度下.向容积为1L的容器中充人3 mol NO和1 mol CO, NO的转化率随时间的变化如下图所示 题目和参考答案——青夏教育精英家教网——
29.碳及其含碳化合物在人们的生产生活中应用广泛. (1)天然气是人们日常生活中的清洁能源. 已知①CH4(g)+2O2(g)=CO2(g)+2 H2O(l), △H1=
甲醇是人们开发和利用的一种新能源.已知:①2H2(g)+O2(g)═2H2O(l)△H1=
消除含氮化合物对大气和水体的污染是环境保护的重要研究课题。(1)已知:反应ⅠN2(g)+O2(g)=2NO(g)ΔH=akJ·mol-1反应Ⅱ2NO(g)+O2
(1)甲烷是一种高效清洁的新能源.0.25mol甲烷完全燃烧生成液态水时.放出222.5kJ热量.则甲烷燃烧热的热化学方为CH4(g)+2O2(g)→CO2(g)+2H2O(l)△H=
利用CO2和CH4重整可制合成气(主要成分为CO.H2).已知重整过程中部分反应的热化学方程式为:①CH4+2H2(g)△H=+75.0KJ•mol
甲烷作为一种新能源在化学领域应用广泛.请回答下列问题:(1)甲烷
甲醇是一种可再生能源,具有广泛的开发和应用前景.(1)工业上一般采用下列两种反应合成甲醇:反应I:CO(g)+2H2(g)CH3OH(g)ΔH1反应II:CO2(g)+3H2(g)CH3OH(g)+H2O(g)ΔH2①上述反应

