LiFePO4锂离子动力电池是奥运会绿色能源.该电池放电时的电极反应式为:正极 FePO4+Li++e
绿色能源储存技术(如锂离子电池)促进了电动车的广泛应用。 #生活知识# #科技生活# #科技改变生活# #新能源科技#
LiFePO4锂离子动力电池是奥运会绿色能源.该电池放电时的电极反应式为:正极 FePO4+Li++e-═LiFePO4,负极 Li-e-═Li+.下列说法中正确的是( )
A、充电时,反应为FePO4+Li=LiFePO4
B、充电时,电池上标注“+”的电极应与外接电源的正极相连
C、放电时,在正极上是Li+得电子被还原
D、放电时,电池内部Li+向正极移动
试题答案在线课程分析:放电时为原电池反应,正极发生还原反应,负极发生氧化反应,原电池工作时,阳离子向正极移动,阴离子向负极移动,充电时,原电池的负极与电源的负极连接,发生还原反应,原电池的正极与电源的正极相连,发生氧化反应,结合电极方程式解答该题.
解答:解:A.由正负极电极方程式可知放电时电池反应为FePO4+Li=LiFePO4,则充电时电池反应为LiFePO4=FePO4+Li,故A错误;
B.充电时动力电池上标注“+”的电极应与外接电源的正极相连,发生氧化反应:LiFePO4-e-=FePO4+Li+,故B正确;
C.放电时,在正极上FePO4得电子被还原,故C错误;
D.放电时电池内部Li+向正极移动,故D正确.
故选BD.
点评:本题考查原电池知识,侧重于电池反应式的书写,注意从氧化还原反应的角度分析,易错点为A,注意审题.
练习册系列答案
相关习题
科目:高中化学来源:题型:阅读理解
(2010?江苏)正极材料为LiCoO2的锂离子电池已被广泛用作便携式电源.但钴的资源匮乏限制了其进一步发展.
(1)橄榄石型LiFePO4是一种潜在的锂离子电池正极材料,它可以通过(NH4)2Fe(SO4)2、H3PO4与LiOH溶液发生共沉淀反应,所得沉淀经80℃真空干燥、高温成型而制得.
①共沉淀反应投料时,不将(NH4)2Fe(SO4)2和LiOH溶液直接混合的原因是
Fe2+在碱性条件下更容易被氧化
Fe2+在碱性条件下更容易被氧化
.
②共沉淀反应的化学方程式为
(NH4)2Fe(SO4)2+LiOH+H3PO4=LiFePO4+2NH4HSO4+H2O
(NH4)2Fe(SO4)2+LiOH+H3PO4=LiFePO4+2NH4HSO4+H2O
.
③高温成型前,常向LiFePO4中加入少量活性炭黑,其作用除了可以改善成型后的LiFePO4的导电性能外,还能
与空气中O2反应,防止LiFePO4中的Fe2+被氧化
与空气中O2反应,防止LiFePO4中的Fe2+被氧化
.
(2)废旧锂离子电池的正极材料试样(主要含有LiCoO2及少量AI、Fe等)可通过下列实验方法回收钴、锂.

①在上述溶解过程中,S2O32-被氧化成SO42-,LiCoO2在溶解过程中反应的化学方程式为
8LiCoO2+Na2S2O3+11H2SO4=4Li2SO4+8CoSO4+Na2SO4+11H2O
8LiCoO2+Na2S2O3+11H2SO4=4Li2SO4+8CoSO4+Na2SO4+11H2O
.
②Co(OH)2在空气中加热时,固体残留率随温度的变化如右图所示.已知钴的氢氧化物加热至290℃时已完全脱水,则1000℃时,剩余固体的成分为
CoO
CoO
.(填化学式);在350~400℃范围内,剩余固体的成分为
Co2O3、Co3O4
Co2O3、Co3O4
.(填化学式).
查看答案和解析>>
科目:高中化学来源:题型:
运用所学的化学反应原理研究化学反应很有意义.请回答下列问题:
(1)合成氨原料中的H2可用甲烷在高温下与水蒸气反应制得.部分1mol物质完全燃烧生成常温下稳定氧化物的△H数据如下表:
已知1mol H2O(g)转变为1molH2O(l)时放热44.0kJ.写出CH4和水蒸气在高温下反应得到CO和H2的热化学方程式
CH4(g)+H2O(g)═CO(g)+3H2(g)△H=+206.1kJ/mol
CH4(g)+H2O(g)═CO(g)+3H2(g)△H=+206.1kJ/mol
.
(2)500°C、50Mpa时,在容积为VL的定容容器中加入n mol N2、3n mol H2,反应达到平衡后N2的转化率为a.则容器内气体的压强反应前与平衡时的比值为
.
(3)若把标准状况下4.48L氨气通入到100g19.6%的硫酸溶液中,所得溶液中的溶质是
NH4HSO4
NH4HSO4
,溶液中离子浓度从大到小的顺序是
c(H+)>c(SO42-)>c(NH+4)>c(OH-)
c(H+)>c(SO42-)>c(NH+4)>c(OH-)
.
(4)某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示.有沉淀析出的是
b
b
点(填字母).a点对应的Ksp 
等于
等于
c点对应的Ksp (填大于、等于或小于)
(5)以磷酸亚铁锂(LiFePO4)为电极材料的新型锂离子电池具有稳定性高、安全、对环境友好等优点,可用于电动汽车.该锂离子电池在充电过程中,阳极的磷酸亚铁锂生成磷酸铁,则该电池放电时正极的电极反应式为
FePO4+Li++e-═LiFePO4
FePO4+Li++e-═LiFePO4
.
查看答案和解析>>
科目:高中化学来源:题型:
(2013?漳州二模)钛铁矿的主要成分为FeTiO3(可表示为FeO?TiO2),含有少量MgO、CaO、SiO2等杂质.利用钛铁矿制备锂离子电池电极材料(钛酸锂Li4Ti5O12和磷酸亚铁锂LiFePO4)的工业流程如图所示: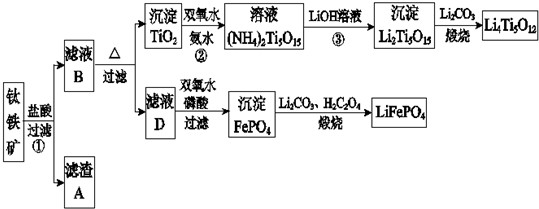
已知:FeTiO3与盐酸反应的离子方程式为:FeTiO3+4H++4Cl-=Fe2++TiOCl42-+2H2O
(1)化合物FeTiO3中铁元素的化合价是
+2
+2
.
(2)滤渣A的成分是
SiO2
SiO2
.
(3)滤液B中TiOCl42-转化生成TiO2的离子方程式是
TiOCl42-+H2O=TiO2↓+2H++4Cl-
TiOCl42-+H2O=TiO2↓+2H++4Cl-
.
(4)反应②中固体TiO2转化成(NH4)2Ti5O15溶液时,Ti元素的浸出率与反应温度的关系如图所示.反应温度过高时,Ti元素浸出率下降的原因是
温度过高时,反应物氨水(或双氧水)受热易分解
温度过高时,反应物氨水(或双氧水)受热易分解
.
(5)反应③的化学方程式是
(NH4)2Ti5O15+2 LiOH=Li2Ti5O15↓+2NH3?H2O(或2NH3+2H2O)
(NH4)2Ti5O15+2 LiOH=Li2Ti5O15↓+2NH3?H2O(或2NH3+2H2O)
.
(6)由滤液D制备LiFePO4的过程中,所需 17%双氧水与H2C2O4的质量比是
20:9
20:9
.
(7)若采用钛酸锂(Li4Ti5O12)和磷酸亚铁锂(LiFePO4)作电极组成电池,其工作原理为:Li4Ti5O12+3LiFePO4?+3FePO4该电池充电时阳极反应式是
LiFePO4-e-=FePO4+Li+
LiFePO4-e-=FePO4+Li+
.
查看答案和解析>>
科目:高中化学来源:题型:
新型LiFePO4可充电锂离子动力电池以其独特的优势成为绿色能源的新宠.已知该电池放电时,正极:FePO4+Li++e-=LiFePO4,负极:Li-e-=Li+.下列说法中正确的是( )
A.充电时动力电池上标注“+”的电极应与外接电源的正极相连
B.充电时电池反应为FePO4+Li++e-=LiFePO4
C.放电时电池内部Li+向负极移动
D.放电时,在正极上Li+得电子被还原
查看答案和解析>>
网址:LiFePO4锂离子动力电池是奥运会绿色能源.该电池放电时的电极反应式为:正极 FePO4+Li++e https://www.yuejiaxmz.com/news/view/262008
相关内容
LiFePO4新型锂离子动力电池以其独特优势成为奥运会绿色能源新宠。已知该电池放电时的电极反应式为:正极FePO4+Li++e[题目]某新型锂离子可充电电池正极材料是含锂的二氧化钴(LiCoO2).充电时LiCoO2被氧化.Li+迁移并以原子形式嵌入电池负极材料碳(C6)中形成LiC6.下列说法正确的是A. 充电时.锂离子电池的负极发生氧化反应B. 放电时.锂离子电池的正极反应为CoO2+Li++e=LiCoO2C. 放电时.锂离子电池的正极的质量逐渐减小D. 充电时.C6极应与 题目和参考答案——青夏教育精英家教网——
磷酸铁锂电池是如何维护的【钜大锂电】
锂电池是一种新型的高能电池.以质量轻.电容量大而备受重视.在手机中被广为使用.目前已制成多种功能的锂电池.其中某种锂电池的总反应可表示为:Li+MnO2=LiMnO2.在上述反应中.锂元素的化合价从 价转变为+1价.锰元素的化合价从 价变为+3价.其中化合价升高的元素是 . 题目和参考答案——青夏教育精英家教网——
锂离子电池=微型炸弹?【钜大锂电】
钠离子电池:未来绿色能源的新选择
废旧锂离子电池绿色再生利用以及衍生产品
“碳呼吸电池 是一种新型能源装置.其工作原理如图.下列说法正确的是( )A.该装置是将电能转变为化学能B.正极的电极反应为:C2O42
能源结构绿色迭代:中国动力电池的低碳之路
动力锂电池日常保养与检修

