可逆反应2SO2+O22SO3.正反应速率分别用v(SO2).v(O2).v(SO3)(mol·L
在夜晚,用反光材料制作V字形,模仿鸟类飞行轨迹 #生活常识# #应急生存技巧# #求生信号#
可逆反应2SO2+O22SO3,正反应速率分别用v(SO2)、v(O2)、v(SO3)(mol·L-1·min-1)表示,逆反应速率分别用v′(SO2)、v′(O2)、v′(SO3)(mol·L-1·min-1)表示,当反应达到化学平衡时,正确的关系是
①v(SO2)=v′(SO2)
②v(O2)=v′(SO2)=v(SO3)
③v(O2)=v′(SO2)
④v′(SO2)=v′(O2)=v′(SO3)
A.①②③④ B.①②③ C.②③④ D.①③
试题答案在线课程D
【解析】根据化学反应速率判断一个反应是否达到化学平衡的标志是:v正=v逆。对于反应2SO2(g)+O2(g)2SO3(g)达到化学平衡时,v(SO2)=2v(O2)=v(SO3)=v′(SO2)=2v′(O2)=v′(SO3)。
练习册系列答案
相关习题
科目:高中化学来源:2014年高一化学人教版必修二 1-1-3原子结构 核素练习卷(解析版)题型:选择题
氧元素有三种核素16O、17O、18O,它们在自然界中所占的原子个数百分比分别为a%、b%、c%,则下列说法正确的是( )
A.一个16O原子的质量为16 g
B.17O的相对原子质量约为17
C.氧元素的相对原子质量为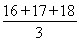
D.氧元素的相对原子质量为(16a%+17b%+18c%)
查看答案和解析>>
科目:高中化学来源:2014年高一化学人教版必修二 1-1-1元素周期表练习卷(解析版)题型:选择题
下图各为元素周期表的一部分(数字为原子序数),其中X为35的是( )
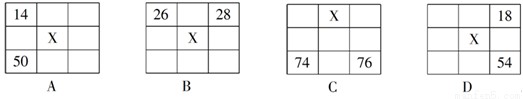
查看答案和解析>>
科目:高中化学来源:2014年高一化学人教版必修2 模块水平检测2练习卷(解析版)题型:选择题
如图所示,杠杆AB两端分别挂有体积相同、质量相等的空心铜球和空心铁球,调节杠杆并使其在水中保持平衡,然后小心地向水槽中滴入浓CuSO4溶液,一段时间后,下列有关杠杆的偏向判断正确的是
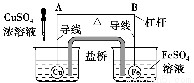
A.杠杆为导体或绝缘体时,均为A端高B端低
B.杠杆为导体或绝缘体时,均为A端低B端高
C.当杠杆为导体时,A端低B端高;杠杆为绝缘体时,A端高B端低
D.当杠杆为导体时,A端高B端低;杠杆为绝缘体时,A端低B端高
查看答案和解析>>
科目:高中化学来源:2014年高一化学人教版必修2 模块水平检测1练习卷(解析版)题型:填空题
某含氧有机物X,其相对分子质量为46,其中碳的质量分数为52.2%,氢的质量分数为13.0%,其余为氧。
(1)X的分子式是________。
(2)X能与金属钠反应放出氢气,则X结构中含有的官能团的名称为________。
(3)X与空气中的氧气在催化剂作用下反应生成了Y,该反应的化学方程式是______________________,反应类型为________。
(4)X与高锰酸钾酸性溶液反应可生成Z,在加热和浓硫酸作用下,X与Z反应可生成一种有香味的物质W,若184 g X和120 g Z反应生成132 g W,该反应的化学方程式为____________________________,其中X的转化率为________。
查看答案和解析>>
科目:高中化学来源:2014年高一化学人教版必修2 模块水平检测1练习卷(解析版)题型:选择题
已知A、B、C、D、E是短周期中原子序数依次增大的5种主族元素,其中元素A、E的单质在常温下呈气态,元素B的原子最外层电子数是其电子层数的2倍,元素C在同周期的主族元素中原子半径最大,元素D的合金是日常生活中常用的金属材料。下列说法正确的是
A.元素A、B组成的化合物常温下一定呈气态
B.一定条件下,元素C、D的最高价氧化物对应的水化物之间能发生反应
C.工业上不能用电解法制备元素C、D、E的单质
D.化合物AE与CE含有相同类型的化学键
查看答案和解析>>
科目:高中化学来源:2014年高一化学人教版必修2 模块水平检测1练习卷(解析版)题型:选择题
化学与能源开发、环境保护、资源利用等密切相关。下列说法正确的是
A.为提高农作物的产量和质量,应大量使用化肥和农药
B.绿色化学的核心是应用化学原理对环境污染进行治理
C.实现化石燃料清洁利用,就无需开发新能源
D.垃圾是放错地方的资源,应分类回收利用
查看答案和解析>>
科目:高中化学来源:2014年高一化学人教版必修2 期中测试练习卷(解析版)题型:选择题
和是铀的两种主要的同位素。是制造原子弹和核反应堆的主要原料,曾经人们觉得没有什么用处,于是就把它叫做贫铀。后来,美国人利用制造了贫铀弹,它具有很强的穿甲能力。下列有关说法正确的是
A.原子核中含有92个中子
B.原子核外有143个电子
C.与互为同位素
D.与互为同素异形体
查看答案和解析>>
科目:高中化学来源:2014年高一化学人教版必修2 4.1.2海水资源的开发利用练习卷(解析版)题型:选择题
海洋中有丰富的食品、矿产、能源、药物和水产资源。下图是从海水中提取某些原料的流程图。
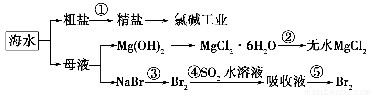
下列有关说法正确的是( )。
A.第①步中除去粗盐中的SO42—、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序为Na2CO3溶液―→NaOH溶液―→BaCl2溶液―→过滤后加盐酸
B.工业上通过氯碱工业制取金属钠
C.从第③步到第⑤步的目的是浓缩、富集溴单质
D.第②步的反应条件是高温加热
查看答案和解析>>
网址:可逆反应2SO2+O22SO3.正反应速率分别用v(SO2).v(O2).v(SO3)(mol·L https://www.yuejiaxmz.com/news/view/313287
相关内容
温度为T时,在两个起始容积都为1L的恒温密闭容器发生反应:H2(g)+I2(g) 2HI(g) ΔH<0。实验测得:v正=v(H2)消耗=v(I2)消耗=k正c(H2)·c(I2),v逆=v(HI)消耗=k逆c2 (HI),在一定条件下.二氧化硫和氧气发生如下反应:2SO2(g)+O2(g)?2SO3(1)写出该反应的化学平衡常数表达式 K= (2)降低温度.该反应K值 .二氧化硫转化率 .化学反应速率 (以上均填增大.减小或不变)(3)600℃时.在一密闭容器中.将二氧化硫和氧气混合.反应过程中SO2.O2.SO3物质的量变化如图.反应处于平衡状态的时间是 .(4)� 题目和参考答案——青夏教育精英家教网——
随着化石能源的减少.新能源的开发利用日益迫切.(1)Bunsen热化学循环制氢工艺由下列三个反应组成:SO2(g)+I2(g)+2H2O+H2SO4(l)△H=a kJ?mol
(1)硝化法是一种古老的生产硫酸的方法.同时实现了氮氧化物的循环转化.主要反应为:NO2SO3 ΔH=
下列离子方程式正确的是( ) A.碳酸钡溶解于稀硝酸中 BaCO3+2H+====Ba2++CO2↑+H2O B.SO2使溴水褪色 SO2+Br2+2H2O====4H++2Br
在四个同样密闭容器中发生反应:A.在同一时间内测得容器内的反应速率:甲为:v,乙为v(B)=4.5mol/=4mol/=0.75mol/.若其它条件相同.温度不同.则温度由低到高的顺序是乙<丙<甲<丁. 题目和参考答案——青夏教育精英家教网——
随着环保意识的增强.清洁能源越来越受人们关注.(1)氢能在二十一世纪有可能在世界能源舞台上成为一种举足轻重的二次能源. 硫
下列有机物命名正确的是 A.CH2=CH
低碳生活是一种时尚的生活理念.倡导人们降碳节能.有效幵发利用CO2.(1) 若用如图装置,以CO2和H2为原料制备甲醇,发生反应为.H2应从电解池的 通入,其中b电极的电极反应方程式为 .(2) 工业上可在6500C浮石银催化作用下用甲醇制备甲醛.当时.制备反应分两步进行.其中一步是.则另一步是 .的HCHO可用于杀菌消毒.其原因是 . 题目和参考答案——青夏教育精英家教网——
甲醇是人们开发和利用的一种新能源.已知:①2H2(g)+O2(g)═2H2O(l)△H1=

