金属单质及其化合物与工农业生产.日常生活有密切的联系.请回答下列问题:(1)一定温度下.氧化铁可以与一氧化碳发生如下反应:Fe2O3+3CO2(g).△H=QkJ?mol
切水果前用水冲一下,可以减少氧化 #生活常识# #日常生活小窍门# #日常生活妙招# #烹饪技巧与食谱#
金属单质及其化合物与工农业生产、日常生活有密切的联系.请回答下列问题: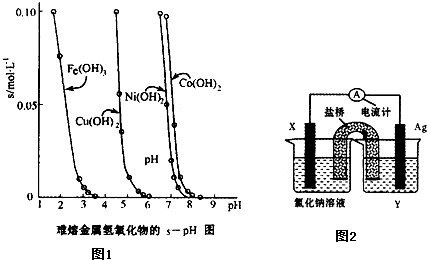
(1)一定温度下,氧化铁可以与一氧化碳发生如下反应:
Fe2O3(s)+3CO(g)?2Fe(s)+3CO2(g),△H=QkJ?mol-1
①该反应的平衡常数表达式K=
;
②该温度时,在2L盛有Fe2O3粉末的密闭容器中通入CO气体,5min后,生成了单质铁11.2g,则这段时间内CO的反应速率为
;
③达平衡后,若温度升高的值增大,则Q
0(填“>”、“=”、“<”).
(2)工业常根据金属氢氧化物在酸中溶解度不同,通过控制溶液的pH,达到分离金属离子的目的.如图1是难溶金属的氢氧化物在不同pH下的溶解情况(s/mol?L-1).若要除去CuCl2溶液的少量Fe3+,应控制溶液的pH为
(填序号).
A.小于1 B.4左右 C.大于6 D.大于9
(3)某工业废水中含有Cu2+、Pb2+、Hg2+,若向工业废水中加入过量的FeS,当FeS、CuS、PbS和HgS共存时,溶液中c(Fe2+):c(Pb2+):c(Hg2+)=
:
:
.已知:Ksp(FeS)=6.3×10-18mol2?L-2,Ksp(PbS)=3.4×10-28mol2?L-2Ksp(CuS)=1.3×10-36mol2?L-2,Ksp(HgS)=6.4×10-53mol2?L-2
(4)依据氧化还原反应:Cu2+(aq)+Fe(s)═Fe2+(aq)+Cu(s)设计成如图2所示的原电池,则关于该电池装置的说法中不正确的是
(填序号).
A.电极X的材料是Fe
B.电解质溶液Y是AgNO3溶液
C.原电池工作时,盐桥中的阴离子不断移向左池的氯化钠溶液中
D.原电池工作时,x电极反应为:O2+2H2O+4e-→4OH-.
分析:(1)①Fe2O3和Fe是固体,不能写在表达式中,故K=;
②n(Fe)=,根据方程式可知n(CO)=n(Fe),故可求得v(CO)
③温度升高的值增大,平衡逆移,故正方向为放热反应;
(2)由图1可知PH在4左右时,Fe3+,完全沉淀,而Cu2+还没开始沉淀;
(3)由Ksp(HgS)=6.4×10-53mol2?L-2求出c(S2-),再分别利用各自的Ksp求出其阳离子浓度.
(4)A.根据图2可知电极X的材料是Fe;
B.电解质溶液Y是AgNO3溶液;
C.原电池工作时,盐桥中的阴离子不断移向负极移动;
D.原电池工作时,x为负极.
解答:解:(1)①Fe2O3和Fe是固体,不能写在表达式中,故K=,故答案为:;
②n(Fe)===0.2mol,根据方程式可知n(CO)=n(Fe)=0.3mol,c(CO)==0.15mol/L,故可求得v(CO)==0.03mol?L-1?min-1,
故答案为:0.03mol?L-1?min-1;
③温度升高的值增大,平衡逆移,则正方向为放热反应,故Q<0,故答案为:<;
(2)由图1可知PH在4左右时,Fe3+,完全沉淀,而Cu2+还没开始沉淀,故答案为:B;
(3)由Ksp(HgS)=6.4×10-53mol2?L-2求出c(S2-)==8×10-27mol?L-1,溶液中c(S2-)相同,再分别利用各自的Ksp求出其阳离子浓度,可求出c(Fe2+):c(Pb2+):c(Hg2+)=6.3:3.4×10-10:6.4×10-35,故答案为:6.3:3.4×10-10:6.4×10-35;
(4)A.根据图2可知电极X的材料是Fe,故A正确;
B.Ag电极应该插入AgNO3溶液,故B正确;
C.原电池工作时,盐桥中的阴离子不断移向负极移动,故C错误;
D.原电池工作时,x为负极,电极反应为:Fe-2e-→Fe2+,故D错误;
故答案为:CD.
点评:本题考查了化学平衡常数、溶度积、原电池等知识,要注意多种离子混合溶液中Ksp的应用.
练习册系列答案
相关习题
科目:高中化学来源:题型:
(2008?闵行区模拟)A、B、C、D是四种短周期元素,它们的相关信息如下表:
元素 元素性质及相关信息 A 其单质的一种晶体虽不是金属晶体,但是电的良导体,且难熔、质软并有润滑性,可作高温轴承的润滑剂、火箭发动机喷管和电极材料. B 其单质能与强酸、强碱溶液反应,其离子在第三周期单核阳离子中半径最小. C 是蛋白质的组成元素之一,原子核外有3种不同能量的电子,且未成对电子数最多. D 原子核外最外层电子排布为nsnnp2n+1.(1)表中所述A的单质晶体中微粒间的相互作用有
共价键
共价键
、
范德华力
范德华力
.
(2)B元素原子核外最外层电子的轨道表示式为


,其最高价氧化物对应水化物的化学特性是
两性氢氧化物(即能与酸反应,又能与碱反应)
两性氢氧化物(即能与酸反应,又能与碱反应)
.
(3)C元素的氢化物的分子为
极性
极性
(填“极性“或”非极性“)分子,其溶于水后溶液呈碱性的原因是
NH3+H2ONH 3?H2ONH4++OH-
NH3+H2ONH 3?H2ONH4++OH-
(用方程式表示).
(4)与D同主族的短周期元素,其单质及其化合物与D的单质及化合物均具有的性质为
A、C
A、C
(填序号).
A.一定条件下其单质易与活泼金属反应 B.气态氢化物极易溶于水并呈强酸性
C.气态氢化物具有很好的热稳定性 D.常温下单质跟水剧烈反应并放出氧气.
查看答案和解析>>
科目:高中化学来源:题型:
金属单质及其化合物在生产生活中应用非常广泛,废旧金属的回收利用是重要研究课题.
某学习小组在实验室中模拟利用含铜废料(主要成分为Cu和CuO,还有少量的Al、Fe及其氧化物)生产胆矾,其实验方案如下: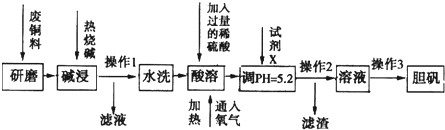
(1)上述流程中,操作1所得“滤液”的主要成分为
;
(2)酸溶后所得溶液中的溶质主要有
;
(3)请写出酸溶过程单质铜发生反应的离子方程式
;该反应中氧化剂与还原剂的物质的量之比为
;
(4)试剂X可以是
;
(5)操作3是一系列操作,其操作为
、冷却结晶、过滤、
、小心干燥;试写出最终产物胆矾的化学式
.
查看答案和解析>>
科目:高中化学来源:2010年四川绵阳高考预测(综合题)化学卷题型:填空题
查看答案和解析>>
科目:高中化学来源:题型:
金属单质及其化合物与工农业生产、日常生活有密切的联系。请回答下列问题:

(2)一定温度下,氧化铁可以与一氧化碳发生如下反应:

①该温度时,在2 L盛有Fe2O3粉末的密闭容器中通入CO气体,5 min后,生成了单质铁11.2 g,则这段时间内CO的反应速率为 ;
②达平衡后,若温度升高,的值增大,则Q 0(填“>”、“=”、“<”)。
(3)工业常根据金属氢氧化物在酸中溶解度不同,通过控制溶液的pH,达到分离金属离子的目的。如是难溶金属的氢氧化物在不同pH下的溶解情况(s/mol·L-1)。若要除去CuCl2溶液的少量Fe3+,应控制溶液的pH为 (填序号)。
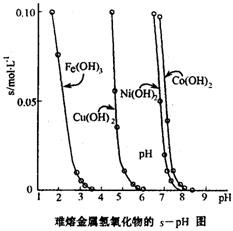
A.小于l B.4左右 C.大于6 D.大于9
(4)某工业废水中含有Cu2+、Pb2+、Hg2+,若向工业废水中加入过量的FeS,当FeS、CuS、PbS和HgS共存时,溶液中c(Fe2+):c(Pb2+):c(Hg2+)= : : 。
已知:Ksp(FeS)=6.3×10-18mol2·L-2,Ksp(PbS)=3.4×10-28mol2·L-2
Ksp(CuS)=1.3×10-36mol2·L-2,Ksp(HgS)=6.4×10-53mol2·L-2
(5)依据氧化还原反应:Cu2+(aq)+Fe(s)===Fe2+(aq)+Cu(s)设计成如图所示的原电池,则关于该电池装置的说法中不正确的是 (填序号)。
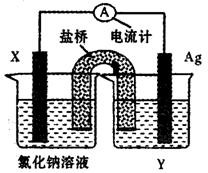
A.电极X的材料是Fe
B.电解质溶液Y是AgNO3溶液
C.原电池工作时,盐桥中的阴离子不断移向左池的氯化钠溶液中
D.原电池工作时,x电极反应为:O2+2H2O+4e-→4OH-
查看答案和解析>>
网址:金属单质及其化合物与工农业生产.日常生活有密切的联系.请回答下列问题:(1)一定温度下.氧化铁可以与一氧化碳发生如下反应:Fe2O3+3CO2(g).△H=QkJ?mol https://www.yuejiaxmz.com/news/view/352253
相关内容
(15分)铁和铁的化合物在工业生产和日常生活中都有广泛的用途,请回答下列问题:(1)铁元素在周期表中的位置是。(2)写出Fe与稀硫酸反应的离子方程式。(3)已知:Fe2O3(s)+C(s)=CO铁是生产生活中应用最广泛的金属.炼铁技术备受关注.已知:①2Fe2O3+3CO2(g)△H=+460.5kJ•mol
铁及其化合物在日常生活.生产中应用广泛.氯化铁和高铁酸钾都是常见的水处理剂.如图为制备氯化铁及进一步氧化制备高铁酸钾的工艺流程.请回答下列问题:(1)已知:①Fe2O3+3CO(g)△H=+489.0kJ•mol
随着化石能源的减少.新能源的开发利用日益迫切.(1)Bunsen热化学循环制氢工艺由下列三个反应组成:SO2(g)+I2(g)+2H2O+H2SO4(l)△H=a kJ?mol
无水AlCl3可用作有机合成的催化剂、食品膨松剂等.工业制备无水AlCl3的流程如下:(1)已知:C(s)+12O2(g)═CO(g)△H=
科学实验和人类的生活经验告诉我们.化学反应中的物质变化和能量变化是紧密地联系在一起的.请回答以下问题:(1)离子反应H+(aq)+OH
甲醇是重要的工业原料.煤化工可以利用煤炭制取水煤气从而合成甲醇:COCH3OH(g).已知①常压下反应的能量变化如图所示.②③CO ΔH=
“低碳生活.绿色出行 .学校建议同学们骑自行车出行.请回答下列问题(1)图中所标示的各部件中.属于金属材料的是 (2)自行车车架一般用生铁制造.某些部件为不锈钢.工业上常以赤铁矿为原料炼铁.请写出一氧化碳与氧化铁在高温下反应的化学方程式: (3)车架表面喷漆不仅美观.而且可有效防止其与 接触而生锈.防止公共自行车链条生锈� 题目和参考答案——青夏教育精英家教网——
铁及其化合物在生产、生活中有广泛应用。请回答下列问题:(1)水热法制备Fe3O4纳米颗粒的反应是:3Fe2++2S2O32
(14分)钢铁生产中的尾气易造成环境污染,清洁生产工艺可消减污染源并充分利用资源。已知:①3Fe2O2(s)+CO(g)2Fe3O2(s)+CO2(g)△H=—47kJ/mol②Fe3O3(s)+3CO(g)2Fe(s)+3CO2(g)△H=—

