甲烷是一种高效清洁的新能源.0.25mol甲烷完全燃烧生成液态水时放出222.5KJ热量.则下列热化学方程式中正确的是A.2CH4(g)+ 4O2(g) == 2CO2(g) + 4H2O(l),ΔH== +890kJ·mol
热水器使用过程中出现异味,可能是燃烧不完全,需清洁 #生活技巧# #家电维护技巧# #热水器故障排除#
 (1)甲烷是一种高效清洁的新能源,0.25mol甲烷完全燃烧生成液态水时,放出222.5kJ热量,则甲烷燃烧热的热化学方为
(1)甲烷是一种高效清洁的新能源,0.25mol甲烷完全燃烧生成液态水时,放出222.5kJ热量,则甲烷燃烧热的热化学方为
CH4(g)+2O2(g)→CO2(g)+2H2O(l)△H=-890KJ/mol
CH4(g)+2O2(g)→CO2(g)+2H2O(l)△H=-890KJ/mol
.
(2)已知:Fe(s)+1/2O2(g)=FeO(s)△H=-270.0kJ/mol,2Al(s)+3/2O2(g)=Al2O3(s)△H=-1675.7kJ/mol,Al和FeO发生铝热反应的热化学方程式是
2Al(s)+3FeO(s)═Al2O3(s)+3Fe(s)△H=-865.7 kJ?mol-1
2Al(s)+3FeO(s)═Al2O3(s)+3Fe(s)△H=-865.7 kJ?mol-1
.
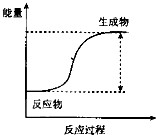
(3)①反应的分类研究:从能量变化角度分,将反应分为放热反应和吸热反应.下列反应中能量变化符合如图所示的是
BC
BC
(填序号)
A.铁片与稀盐酸反应
B.灼热的碳与CO2反应
C.Ba(OH)2?8H2O与NH4Cl反应
D.甲烷在氧气中的燃烧反应
②煤作为燃料有两种途径:
Ⅰ、C(s)+O2(g)═CO2(g)△H1<0Ⅱ.C(s)+H2O(g)═CO(g)+H2(g)△H2>0
2CO(g)+O2(g)═2CO2(g)△H3<0 2H2(g)+O2(g)═2H2O(g)△H4<0
请回答:途径Ⅰ放出的热量
=
=
途径Ⅱ放出的热量(填“>”、“<”或“=”).
△H1、△H2、△H3、△H4之间关系的数学表达式是
△H1=△H2+(△H3+△H4)
△H1=△H2+(△H3+△H4)
.
网址:甲烷是一种高效清洁的新能源.0.25mol甲烷完全燃烧生成液态水时放出222.5KJ热量.则下列热化学方程式中正确的是A.2CH4(g)+ 4O2(g) == 2CO2(g) + 4H2O(l),ΔH== +890kJ·mol https://www.yuejiaxmz.com/news/view/473868
相关内容
甲烷是一种高效清洁的新能源,0.25mol甲烷完全燃烧生成液态水时放出222.5KJ热量,则下列热化学方程式中正确的是[]A.2CH4(g)+4O2(g)==2CO2(g)+4H2O(l)ΔH==+890kJ·mol甲烷是一种高效清洁的新能源.0.25mol甲烷完全燃烧生成液态水时放出222.5kJ热量.则表示甲烷燃烧热的热化学方程式为( )A.2CH4(g)+4O2(g)?2CO2(g)+4H2O(l)△H=+——青夏教育精英家教网——
甲烷是一种高效清洁的新能源.0.25mol甲烷完全燃烧生成液态水时放出222.5kJ热量.则下列热化学方程式中正确的是A.2CH4(g) + 4O2(g) = = 2CO2(g) + 4H2O(l) ΔH= +890 kJ·mol
甲烷是一种高效清洁的新能源.0.25 mol甲烷完全燃烧时放出222.5 kJ热量.则下列热化学方程式中正确的是 A.2CH4(g)+4O2(g)====2CO2(g)+4H2O(l) ΔH=+890 kJ·mol
甲烷是一种高效清洁的新能源,0.25mol甲烷完全燃烧生成液态水时放出222.5kJ热量,则表示甲烷燃烧热的热化学方程式为( )A. 2CH4(g)+4O2(g)═2CO2(g)+4H2O(l)△H=+890kJ•mol
甲烷是一种高效清洁的新能源.0.25mol甲烷完全燃烧生成液态水时放出222.5KJ热量.则下列热化学方程式中正确的是( ) A.2CH4(g) + 4O2(g) = 2CO2(g) + 4H2O(l),ΔH= +890KJ・mol1 B. CH4(g) + 2O2(g) = CO2(g) +2H2O(l), ΔH=+890KJ・mol1 C. CH4 题目和参考答案——青夏教育精英家教网——
(1)甲烷是一种高效清洁的新能源.0.25mol甲烷完全燃烧生成液态水时.放出222.5kJ热量.则甲烷燃烧热的热化学方为CH4(g)+2O2(g)→CO2(g)+2H2O(l)△H=
N2H4是一种高效清洁的火箭燃料.0.25 mol N2H4(g)完全燃烧生成氮气和气态水时.放出133.5 kJ热量.则下列热化学方程式的书写正确的是A.N2H4(g)+O2(g)====N2 (g)+ H2O (g),ΔH=
N2H4是一种高效清洁的火箭燃料.0.25 mol N2H4(g)完全燃烧生成氮气和气态水时.放出133.5 kJ热量.则下列热化学方程式中正确的是A.1/2N2H4(g)+1/2O2(g)=1/2N2(g)+H2O(g) ΔH=+267 kJ·mol
N2H4是一种高效清洁的火箭燃料.0.25 mol N2H4(g)完全燃烧生成氮气和气态水时.放出133.5 kJ热量.则下列热化学方程中正确的是A.1/2 N2H4(g)+ 1/2 O2(g)= 1/2 N2(g)+ H2O(l)△H=+257kJ·mol

