环氧乙烷是高效消毒剂,可用于口罩等医用品消毒,工业常用乙烯氧化法生产。主反应:2CH2=CH2(g)+O2(g)ΔH1=−209.8kJ∙mol−1,副反应:C
用过氧乙酸溶液拖地,能高效消灭病毒 #生活技巧# #家居清洁技巧# #家庭消毒常识#
题型:填空题 难度:0.85 引用次数:173 题号:16735407
环氧乙烷是高效消毒剂,可用于口罩等医用品消毒,工业常用乙烯氧化法生产。
主反应:2CH2=CH2(g)+O2(g) 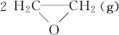 ΔH1=−209.8 kJ∙mol−1,
ΔH1=−209.8 kJ∙mol−1,
副反应:CH2=CH2(g)+3O2(g)=2CO2(g)+2H2O(g) ΔH2=−1323.0 kJ∙mol−1,已知:C2H4的燃烧热ΔH=−1411.0 kJ∙mol−1,则环氧乙烷(g)的燃烧热ΔH=
。
更新时间:2022/09/11 12:19:02 |
抱歉! 您未登录, 不能查看答案和解析点击登录
相似题推荐【推荐1】在环境污染和能源危机日益严重的情况下,氢气作为很有发展前景的新型能源备受青睐,获取氢气的方式有很多。
(1)正丁烷(C4H10)脱氢制1-丁烯(C4H8)的热化学方程式如下:
已知:①C4H10(g)=C4H8(g)+H2(g) ΔH1
②C4H10(g)+O2(g)=C4H8(g)+H2O(g) ΔH2=-119 kJ·mol-1
③H2(g)+O2(g)=H2O(g) ΔH3=-242kJ·mol-1
计算反应①的ΔH1=
。
(2)如图为两种制备氢气的方法。
①书写系统(Ⅰ)和系统(Ⅱ)制氢的热化学方程式
。
②若制得等量H2时,比较两种系统所需能量的大小
。
【推荐2】热化学方程式的书写
(1)1 g碳(s)与适量水蒸气完全反应生成CO(g)和H2(g),需要吸收10.94 kJ热量,该反应的热化学方程式为
。
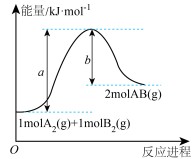
(2)已知某反应的能量变化如图所示,请写出该反应的热化学方程式:
。
(3)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) ΔH=−1275.6
②H2O(l)=H2O(g) ΔH=+44.0
写出表示甲醇燃烧热的热化学方程式
。
(4)图为ⅥA族元素氢化物a、b、c、d的生成热数据示意图。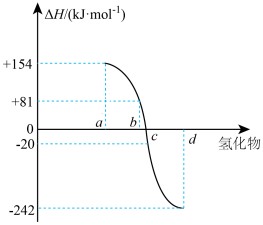
则硫化氢在上述条件下发生分解反应的热化学方程式为
。
【推荐3】已知:Cl2(g)+2NaOH(aq)=NaCl(aq)+NaClO(aq)+H2O(l) △Q1= 102 kJ·mol-1
3Cl2(g)+6NaOH(aq)=5NaCl(aq)+NaClO3(aq)+3H2O(1) △Q2= 422 kJ·mol-1
写出在溶液中NaClO分解生成NaClO3的热化学方程式
。
网址:环氧乙烷是高效消毒剂,可用于口罩等医用品消毒,工业常用乙烯氧化法生产。主反应:2CH2=CH2(g)+O2(g)ΔH1=−209.8kJ∙mol−1,副反应:C https://www.yuejiaxmz.com/news/view/642844
相关内容
丙烯是重要的有机化工原料,丁烯催化裂解法是一种重要的丙烯生产法,生产过程中会有生成乙烯的副反应发生。反应如下:I主反应,3C4H8(g)=4C3H6(g)△H1消除含氮化合物对大气和水体的污染是环境保护的重要研究课题。(1)已知:反应ⅠN2(g)+O2(g)=2NO(g)ΔH=akJ·mol-1反应Ⅱ2NO(g)+O2
甲醇是一种可再生能源,具有广泛的开发和应用前景.(1)工业上一般采用下列两种反应合成甲醇:反应I:CO(g)+2H2(g)CH3OH(g)ΔH1反应II:CO2(g)+3H2(g)CH3OH(g)+H2O(g)ΔH2①上述反应
研究含氮污染物的治理是环保的一项重要工作.合理应用和处理氮的化合物.在生产生活中有重要意义.=2NO(g) △H=+180.5kJ•mol﹣12C △H=﹣221.0kJ•mol﹣1C △H=﹣393. 5kJ•mol﹣1则汽车尾气处理的反应之一:2NO+2CO2(g)△H= kJ•mol﹣1.利于该� 题目和参考答案——青夏教育精英家教网——
生活中到处有化学知识,家用消毒柜常用臭氧(O3)消毒,已知在消毒过程中,通过放电发生如下反应:3O2(g)=2O3(g);△H=+144.8kJ/mol;下列关于臭氧说法不正确的是[]A.O2和O3互为
17.氢气(H2)一氧化碳(CO).辛烷(C8H15).甲烷(CH4)的热化学方程式分别为: H2(g)+O2(g)====H2O(1); △H=
随着化石能源的减少.新能源的开发利用日益迫切.(1)Bunsen热化学循环制氢工艺由下列三个反应组成:SO2(g)+I2(g)+2H2O+H2SO4(l)△H=a kJ?mol
甲烷作为一种新能源在化学领域应用广泛.请回答下列问题:(1)甲烷
氢气是一种清洁能源.氢气的制取与储存是氢能源利用领域的研究热点.(1)以甲烷为原料制取氢气是工业上常用的制氢方法.已知:CH4(g)+H2O+3H2(g) ΔH=+206.2 kJ/molCH4——青夏教育精英家教网——
利用CO2和CH4重整可制合成气(主要成分为CO.H2).已知重整过程中部分反应的热化学方程式为:①CH4+2H2(g)△H=+75.0KJ•mol

