温度为T时,在两个起始容积都为1L的恒温密闭容器发生反应:H2(g)+I2(g) 2HI(g) ΔH<0。实验测得:v正=v(H2)消耗=v(I2)消耗=k正c(H2)·c(I2),v逆=v(HI)消耗=k逆c2 (HI),
1.
(2018·江苏模拟) 温度为T时,在两个起始容积都为1L的恒温密闭容器发生反应:H2(g)+I2(g) 2HI(g) ΔH<0。实验测得:v正=v(H2)消耗=v(I2)消耗=k正c(H2)·c(I2),v逆=v(HI)消耗=k逆c2 (HI),k正、k逆为速率常数,受温度影响。下列说法正确的是( )
容器
物质的起始浓度(mol·L-1)
物质的平衡浓度
c(H2)
c(I2)
c(HI)
Ⅰ(恒容)
0.1
0.1
0
c(I2)=0.07 mol·L-1
Ⅱ(恒压)
0
0
0.6
A . 反应过程中,容器Ⅰ与容器Ⅱ中的总压强的比为1:3 B . 两容器达平衡时:c(HI,容器Ⅱ)>3c(HI,容器Ⅰ) C . 温度一定,容器Ⅱ中反应达到平衡时(平衡常数为K),有K= 成立 D . 达平衡时,向容器Ⅰ中同时再通入0.1 mol I2和0.1 mol HI,则此时ν正>ν逆
【知识点】
能力提升 变式训练 拓展培优 换一批
2.
Deacon法制备Cl2的反应为4HCl(g)+O2(g)⇌2Cl2(g)+2H2O(g)。如图为恒容容器中,进料浓度比c(HCl)∶c(O2)分别等于1∶1、4∶1、7∶1时HCl平衡转化率随温度变化的关系。下列说法正确的是( )
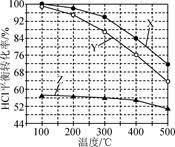
A . 反应4HCl(g)+O2(g)⇌2Cl2(g)+2H2O(g)的ΔH>0 B . Z曲线对应进料浓度比c(HCl)∶c(O2)=7∶1 C . 400 ℃,进料浓度比c(HCl)∶c(O2)=4∶1时,O2平衡转化率为19% D . 400 ℃,进料浓度比c(HCl)∶c(O2)=1∶1时,c起始(HCl)=c0 mol·L-1 , 平衡常数K= 
3.
在密闭容器中:按CO2与H2的物质的量之比为1:3进行投料,发生反应2CO2(g)+6H2(g) CH3CH2OH(g)+3H2O(g) △H<0,在5MPa 下测得不同温度下平衡体系中各种物质的体积分数 ( V% ) 如图所示,下列说法中正确的是( )
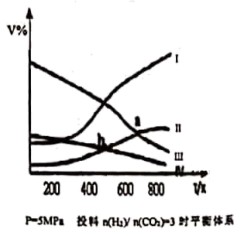
A . 表示CH3CH2OH组分的曲线是IV B . 图中曲线交点a、b 对应的上述反应平衡常数Ka > Kb C . 图中曲线交点a 对应的 CO2 转化率为 40% D . 若甲、乙两个密闭容器起始时的容积、温度及投料方式均相同,甲:恒温恒压,乙;恒温恒容,反应达平衡时CH3CH2OH产率:甲<乙
网址:温度为T时,在两个起始容积都为1L的恒温密闭容器发生反应:H2(g)+I2(g) 2HI(g) ΔH<0。实验测得:v正=v(H2)消耗=v(I2)消耗=k正c(H2)·c(I2),v逆=v(HI)消耗=k逆c2 (HI), https://www.yuejiaxmz.com/news/view/65258
相关内容
低碳生活是一种时尚的生活理念.倡导人们降碳节能.有效幵发利用CO2.(1) 若用如图装置,以CO2和H2为原料制备甲醇,发生反应为.H2应从电解池的 通入,其中b电极的电极反应方程式为 .(2) 工业上可在6500C浮石银催化作用下用甲醇制备甲醛.当时.制备反应分两步进行.其中一步是.则另一步是 .的HCHO可用于杀菌消毒.其原因是 . 题目和参考答案——青夏教育精英家教网——下列有机物命名正确的是 A.CH2=CH
铁是生产生活中应用最广泛的金属.炼铁技术备受关注.已知:①2Fe2O3+3CO2(g)△H=+460.5kJ•mol
(已知:HAc Ka=1.76×10
初三物理知识点总结2024
日常生活、生产中甲烷既是重要的清洁能源也是一种重要的化工原料.(1)如图1是CH4/H2O体系放氢焓变示意图:则CH4(g)+CO2(g)=2CO(g)+2H2(g)△H=
初三物理知识点总结18篇
初三物理的知识点总结
一是“浸没 状态.是指 ,二是物体的一部分体积浸在液体里.另一部分 . (2)G排是指被物体 .F浮=G排表示 . (3)V排表示 .V排与物体的体积V物既有联系.又有区别.当物体全部浸没在液体中时.V排 V物,当物体只有一部分浸在液体中时.V排 V物. (4)由F 题目和参考答案——青夏教育精英家教网——
如图所示为一列简谐横波沿

