日常生活、生产中甲烷既是重要的清洁能源也是一种重要的化工原料。 (1)下图是CH4/H2O体系放氢焓变示意图: 则CH4(g)+CO2(g)=2CO(g)+2H2(g) △H= 。 (2)合成气(CO、H2)
音乐创作中,有时候无意间产生的错误也会变成一种独特的幽默元素,比如巴赫的‘G弦上的咏叹调’。 #生活乐趣# #日常生活趣事# #音乐欣赏的乐趣# #音乐幽默故事#
题目
举报
日常生活、生产中甲烷既是重要的清洁能源也是一种重要的化工原料。
(1)下图是CH4/H2O体系放氢焓变示意图:
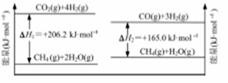
则CH4(g)+CO2(g)=2CO(g)+2H2(g) △H= 。
(2)合成气(CO、H2)是一种用途相当广泛的化工基础原料,常被用来合成很多有机物,如甲醇(CH3OH)、二甲醚(CH3OCH3)等。
①在压强为0.1MPa条件下,物质的量之比为1:3的CO、H2的混合气体在催化剂作用下能自发反应生成甲醇:CO(g)+2H2(g)CH3OH(g) △H<0。若容器体积不变,改变下列条件新平衡下甲醇体积分数增大的是 (填字母)。
A. 升高温度 B. 将CH3OH(g)从体系中分离
C. 充入N2使体系总压强增大 D. 再充入1mol CO和3mol H2
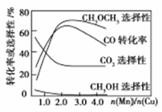 ②二甲醚被誉为“21世纪的清洁燃料”。一定条件下利用H2、CO合成CH3OCH3。其反应方程式为:3H2(g)+3CO(g)CH3OCH3(g)+CO2(g),该反应的平衡常数表达式为 。最近研究发现一种新型的催化剂(主要成分是Cu、Mn的合金)对CO和H2合成二甲醚具有较好的催化效率。根据如图判断,催化剂中n(Mn)/n(Cu)约为 时最有利于二甲醚的合成。
②二甲醚被誉为“21世纪的清洁燃料”。一定条件下利用H2、CO合成CH3OCH3。其反应方程式为:3H2(g)+3CO(g)CH3OCH3(g)+CO2(g),该反应的平衡常数表达式为 。最近研究发现一种新型的催化剂(主要成分是Cu、Mn的合金)对CO和H2合成二甲醚具有较好的催化效率。根据如图判断,催化剂中n(Mn)/n(Cu)约为 时最有利于二甲醚的合成。
③以甲醇为原料是合成二甲醚的又一途径:2CH3OH(g)CH3OCH3(g)+H2O(g)。一定温度下,向2L某容器中充入一定量的CH3OH,10s到达平衡后测得CH3OH 0.04mol,CH3OCH3 0.08mol,则用甲醇表示反应在10s内的平均反应速率为 ,相同条件下起始时向该容器中充入CH3OH 0.15mol、CH3OCH3 0.15mol、和H2O 0.10mol,则反应将向 方向进行(填“正反应”或“逆反应”)。

扫码下载作业帮
搜索答疑一搜即得
答案解析
查看更多优质解析
解答一
举报
(1)+123.8kJ·mol-1(3分) (2)①D(2分) ②(2分) 2.0(2分) ③0.008mol·L―1·s―1(2分) &nb...
解析看不懂?免费查看同类题视频解析
查看解答
特别推荐

网址:日常生活、生产中甲烷既是重要的清洁能源也是一种重要的化工原料。 (1)下图是CH4/H2O体系放氢焓变示意图: 则CH4(g)+CO2(g)=2CO(g)+2H2(g) △H= 。 (2)合成气(CO、H2) https://www.yuejiaxmz.com/news/view/874487
相关内容
日常生活、生产中甲烷既是重要的清洁能源也是一种重要的化工原料.(1)如图1是CH4/H2O体系放氢焓变示意图:则CH4(g)+CO2(g)=2CO(g)+2H2(g)△H=利用CO2和CH4重整可制合成气(主要成分为CO.H2).已知重整过程中部分反应的热化学方程式为:①CH4+2H2(g)△H=+75.0KJ•mol
碳及其含碳化合物在人们的生产生活中应用广泛。(1)天然气是人们日常生活中的清洁能源。已知①CH4(g)+2O2(g)=CO2(g)+2H2O(l);△H1=-890.3kJ·mol-1②2CO(g)+O2(g)=2CO2(g);△H2=
(1)甲烷是一种高效清洁的新能源.0.25mol甲烷完全燃烧生成液态水时.放出222.5kJ热量.则甲烷燃烧热的热化学方为CH4(g)+2O2(g)→CO2(g)+2H2O(l)△H=
随着环保意识的增强,清洁能源越来越受人们关注。(1)甲烷是一种洁净能源,已知:CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=
甲烷是一种高效清洁的新能源.0.25mol甲烷完全燃烧生成液态水时放出222.5KJ热量.则下列热化学方程式中正确的是( ) A.2CH4(g) + 4O2(g) = 2CO2(g) + 4H2O(l),ΔH= +890KJ・mol1 B. CH4(g) + 2O2(g) = CO2(g) +2H2O(l), ΔH=+890KJ・mol1 C. CH4 题目和参考答案——青夏教育精英家教网——
开发使用清洁能源.发展“低碳经济 正成为科学家研究的主要课题.氢气.甲醇是优质的清洁燃料.可制作燃料电池.(1)甲烷水蒸气转化法制H2的主要转化反应如下:CH4(g) + H2O(g) CO(g) + 3H2(g)? △H=+206.2 kJ·mol
29.碳及其含碳化合物在人们的生产生活中应用广泛. (1)天然气是人们日常生活中的清洁能源. 已知①CH4(g)+2O2(g)=CO2(g)+2 H2O(l), △H1=
17.氢气(H2)一氧化碳(CO).辛烷(C8H15).甲烷(CH4)的热化学方程式分别为: H2(g)+O2(g)====H2O(1); △H=
甲烷是一种高效清洁的新能源.0.25mol甲烷完全燃烧生成液态水时放出222.5kJ热量.则下列热化学方程式中正确的是A.2CH4(g) + 4O2(g) = = 2CO2(g) + 4H2O(l) ΔH= +890 kJ·mol

