加碘食盐中含有碘酸钾.现以电解法制备碘酸钾.实验装置如图所示.先将一定量的碘溶于过量氢氧化钾溶液.发生反应:3I2+6KOH=5KI+KIO3+3H2O.将该溶液加入阳极区.另将氢氧化钾溶液加入阴极区.开始电解.下列说法中正确的是A.电解过程中OH
对于碘渍,用酒精或过氧化氢溶液处理效果好 #生活技巧# #衣物护理建议# #颜色衣物去渍#
加碘食盐中含有碘酸钾(KIO3),现以电解法制备碘酸钾,实验装置如图所示。先将一定量的碘溶于过量氢氧化钾溶液,发生反应:3I2+6KOH=5KI+KIO3+3H2O,将该溶液加入阳极区,另将氢氧化钾溶液加入阴极区,开始电解。下列说法中正确的是
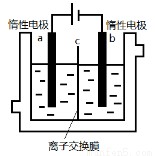
A.电解过程中OH-从a极区通过离子交换膜c进入b极区
B.随着电解进行,KOH溶液浓度会逐渐减小
C.当阳极有0.1mol I-放电时,阴极生成6.72LH2
D.a电极反应式:I- -6e-+6OH-=IO3-+3H2O,a极区的KI最终转变为KIO3
练习册系列答案
相关习题
科目:高中化学来源:2015-2016学年江苏省泰州市姜堰区高二上学期期中选修化学试卷(解析版)题型:选择题
下列做法不利于“开源节流”的是
A.开发太阳能、水能、风能、地热能等新能源
B.大力开采煤、石油和天然气,以满足人们日益增长的能源需求
C.大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源
D.减少资源消耗,注重资源的重复使用、资源的循环再生
查看答案和解析>>
科目:高中化学来源:2016届山东省高三上学期第一次月考化学试卷(解析版)题型:填空题
(11分) 铁是人类较早使用的金属之一。运用铁及其化合物的有关知识,同答下列问题:
(1)铁和铁合金是生活中的常用材料,下列叙述中,正确的是________。(填序号)
A.纯铁硬度比生铁高
B.纯铁耐腐蚀性强,不易生锈
C.不锈钢是铁合金,只含金属元素
D.铁在一定条件下,可与水蒸气反应
E.铁在冷的浓硫酸中钝化
(2)向沸水中逐滴滴加1molL-1FeCl3溶液,至液体呈透明的红褐色,该反应的离子方程式为 ,所形成该分散系的微粒粒度范围是 。
(3)电子工业需用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路极。请写出FeCl3溶液与铜反应的离子方程式 。欲从腐蚀后的废液中回收铜并重新获得FeCl3溶液,现有下列试剂:①氯气②铁粉③浓硝酸④浓盐酸⑤烧碱⑥浓氨水,需要用到的一组试剂是_____________。
A.①②④ B.①③④⑥ C.②④⑤ D.①④⑥
(4)高铁酸钠(Na2FeO4)是一种新型净水剂。
①高铁酸钠主要通过如下反应制取:2Fe(OH)3+3X+4NaOH=2Na2FeO4+3NaCl+5H2O,则X的化学式为 。
②高铁酸钠在水中可以发生如下反应:4FeO4+10H2O==4Fe(OH)3+8OH+3O2↑。由此看来,高铁酸钠能够杀菌消毒是因为它具有___________性,而能够除去水中悬浮物是因为 。
③下列物质能用作净水剂的有___________。
a.KAl(SO4)2l2H2O
b.聚合硫酸铁
c.ClO2
d.“84”消毒液
查看答案和解析>>
科目:高中化学来源:2015-2016学年安徽省高一上学期第一次月考化学试卷(解析版)题型:选择题
相同质量的SO2和SO3它们之间的关系是
A.体积之比为5:4 B.分子数之比为1:1
C.物质的量之比为5:4 D.氧原子的个数比为2:3
查看答案和解析>>
科目:高中化学来源:2016届山东省青岛市高三上学期10月月考化学试卷(解析版)题型:实验题
实验室配制500mL0.2mol•L﹣1的FeSO4溶液,具体操作步骤为:
①在天平上称取一定质量的绿矾(FeSO4•7H2O),把它放在烧杯中,用适量的蒸馏水使其完全溶解;
②把制得的溶液小心的注入500mL的容量瓶中;
③继续向容量瓶中滴加蒸馏水至液面距刻度线1~2cm处时,改用胶头滴管小心滴加,直到溶液的凹液面恰好与刻度线相切为止;
④用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次的洗涤液都转入容量瓶中,并轻轻摇匀;
⑤将容量瓶塞好,充分摇匀。
请填写下列空白.
(1)用托盘天平称取的绿矾的质量为: ;
(2)上述操作的正确顺序为: ;
(3)本次实验过程中多次用到玻璃棒,在溶解时玻璃棒的作用是: ,在移液时玻璃棒的作用是: .
(4)观察液面时,若俯视刻度线,会使所配制的溶液的浓度 (填“偏高”、“偏低”或“无影响”下同);加蒸馏水时不慎超过了刻度线后倒出部分溶液,使液面与刻度线相切,会 ;
(5)用ρ=1.84g•mL﹣1,质量分数为98%的浓硫酸配制200mL1mol•L﹣1的稀硫酸与上述配制溶液的步骤上的差别主要有三点:
①计算:理论上应取浓硫酸的体积V= mL(精确到小数点后两位);
②量取:由于量筒是一种粗略的量具,如想精确量取,必需选用 (填仪器名称).
③溶【解析】
稀释浓硫酸的方法 .
查看答案和解析>>
科目:高中化学来源:2016届浙江省宁波市高三上学期10月月考化学试卷(解析版)题型:选择题
下列说法正确的是
A.HF、HCl、HBr、HI的热稳定性依次减弱,沸点却依次升高
B.熔融状态下能导电的化合物一定含离子键
C.H2O2分子中所有的原子均为8电子稳定结构
D.NaHSO4晶体中阴、阳离子的个数是1:2且熔化时破坏的是离子键和共价键
查看答案和解析>>
科目:高中化学来源:2015-2016学年安徽师大附属中学高二上期中测试化学试卷(解析版)题型:推断题
(16分)Ⅰ.页岩气是一种从页岩层中开采出来的气体资源。以页岩气的主要成分A为原料可合成一种重要的化工产品——乌洛托品,其合成路线如下:
ABC…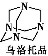
已知A是一种烃,所含碳的质量分数为75%,B的相对分子质量为50.5。
(1)乌洛托品的化学式为
(2)A→B 的化学方程式为 ,其反应类型为
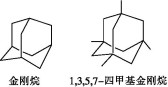
(3)金刚烷和1,3,5,7-四甲基金刚烷(如图)都是结构与乌洛托品相似的有机物,金刚烷与1,3,5,7-四
甲基金刚烷的相对分子质量相差
(4)将甲醛(HCHO)水溶液与氨水混合蒸发也可制得乌洛托品。若原料完全反应生成乌洛托品,则甲
醛与氨的物质的量之比为
A.1:1 B.2:3 C.3:2 D.2:1
Ⅱ.工业上可通过下列途径制备金刚烷:
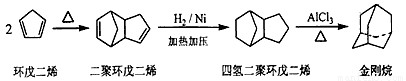
(5)环戊二烯分子中最多有________个原子共平面,金刚烷的二氯代物共有 种
(6)W是二聚环戊二烯的同分异构体,不能使溴的四氯化碳溶液褪色,核磁共振氢谱显示有4组峰,
且峰面积比为3:1:1:1,W经高锰酸钾酸性溶液加热氧化可以得到邻苯二甲酸。写出W可能的
一种结构简式:
查看答案和解析>>
科目:高中化学来源:2015-2016学年江苏省高二上期中选修化学试卷(解析版)题型:选择题
在容积相同的两个密闭容器A和B中,保持温度为423K,同时向A、B中分别加入amol及bmol HI(a>b),可逆反应2HI H2+I2(g)达到平衡后,下列说法正确的是
A.开始时A容器中的反应速率大于B容器中的反应速率
B.平衡时c(I2)A=c(I2)B
C. HI的平衡分解率:αA>αB
D.平衡时,I2蒸气在混合气体中的体积分数:A容器>B容器
查看答案和解析>>
科目:高中化学来源:2016届河南省林州市高三上学期9月质检化学试卷(解析版)题型:选择题
已知饱和酸(A)与足量的乙醇(B)在一定条件下生成酯(C),若M(C)=M(A)+56且A分子比B分子多3个碳原子,则上述反应生成的C最多有
A.4种 B.5种 C.6种 D.7种
查看答案和解析>>
网址:加碘食盐中含有碘酸钾.现以电解法制备碘酸钾.实验装置如图所示.先将一定量的碘溶于过量氢氧化钾溶液.发生反应:3I2+6KOH=5KI+KIO3+3H2O.将该溶液加入阳极区.另将氢氧化钾溶液加入阴极区.开始电解.下列说法中正确的是A.电解过程中OH https://www.yuejiaxmz.com/news/view/244778
相关内容
利用电解法可将含有Fe.Zn.Ag.Pt等杂质的粗铜提纯.下列叙述正确的是 A.电解时可以精铜为阳极.以CuSO4溶液为电解液B.电解时阴极发生还原反应C.粗铜连接电源负极.其电极反应是Cu已知:在氢氧化钠浓溶液中加入氧化钙.加热.制成的白色固体就是碱石灰.有两个实验小组的同学决定通过实验探究碱石灰的组成.(1)第一小组设计方案的流程如下:①写出n (OH
利用右图所示装置可吸收SO2.并用阴极排出的溶液吸收NO2.下列说法正确的是A.a为直流电源的负极B.阴极的电极反应式为:2HSO+2H++e
15.亚硫酸钠在空气中易被氧化生成硫酸钠.现有ag亚硫酸钠样品.溶解后加入足量氯化钡溶液.可得干燥沉淀bg. (1)若亚硫酸钠未被氧化.b= a. (2)若亚硫酸钠全被氧化.b= a.——青夏教育精英家教网——
氢氧化镍[Ni(OH)2]是某种混合动力汽车电池的一种材料.请参与下列探究:[查阅资料]Ⅰ.氢氧化是一种蓝绿色微溶于水的固体,硫酸镍溶液呈绿色,碳酸镍是一种浅绿色固体.Ⅱ.能溶于水的酸.碱.盐溶于水时能电离成离子即以离子的形式存在.如:H2SO4=2H++SO42
“碳呼吸电池 是一种新型能源装置.其工作原理如图.下列说法正确的是( )A.该装置是将电能转变为化学能B.正极的电极反应为:C2O42
下列各组物质能在pH=1的无色溶液中大量共存的是( ) A.K2SO4
[题目]“84消毒液 广泛应用于杀菌消毒.其有效成分是NaClO.实验小组制备消毒液.并利用其性质探索制备碘水的方法.资料:i.HClO的电离常数为Ka=4.7×10
下列图象能正确反映其对应的实验操作的是( )A.向盛有部分变质的氢氧化钠溶液的烧杯中滴加稀硫酸至过量B.向盛有一定量的氢氧化钠溶液的烧杯中逐滴加入pH=2的稀盐酸至过量C.相同质量的镁.锌分别与足量的溶质质量分数相同的稀盐酸反应D.向含有稀盐酸和氯化铜的混合溶液中滴加NaOH溶液 题目和参考答案——青夏教育精英家教网——
金属在日常生活中应用广泛.(1)用锌片和硫酸铜溶液的反应可呈现“铁树开花 的美景.该反应的化学方程式是 .(2)铁制品在喷漆前需放入稀盐酸中除锈.除铁锈的化学方程式是 . Zn + CuSO4 === ZnSO4 + Cu Fe2O3 + 6HCl === 2FeCl3 + 3H2O [解析] (1)锌和硫酸铜反应生成硫酸锌和铜.反应的化学方程式是Zn + 题目和参考答案——青夏教育精英家教网——

