已知:在氢氧化钠浓溶液中加入氧化钙.加热.制成的白色固体就是碱石灰.有两个实验小组的同学决定通过实验探究碱石灰的组成.(1)第一小组设计方案的流程如下:①写出n (OH
已知:在氢氧化钠浓溶液中加入氧化钙,加热,制成的白色固体就是碱石灰.有两个实验小组的同学决定通过实验探究碱石灰的组成.
(1)第一小组设计方案的流程如下: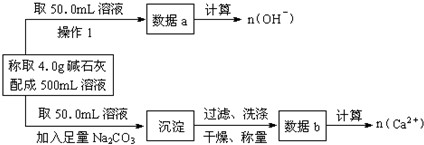
①写出n (OH-)、n (Ca2+)与n (Na+)的关系:n(Na+)=
n(OH-)-2n(Ca2+)
n(OH-)-2n(Ca2+)
.
②设n (Na+)=x mol、n (Ca2+)=y mol,请填写下表:
可能组成 NaOH、CaO NaOH、CaO、
Ca (OH)2 NaOH、
Ca (OH)2 NaOH、
Ca (OH)2、H2O n (Na+)、n (Ca2+)
的关系 40x+56y=4
40x+56y<4.0<40x+74y
40x+56y<4.0<40x+74y
40x+74y=4.0
40x+74y=4.0
40x+74y<4.0
40x+74y<4.0
(2)第二小组同学查得如下资料:Ca(OH)2在250℃时不分解、NaOH在580℃时不分解.
他们设计了如下方案并得出相关数据:取市售碱石灰4.0g,在250℃时加热至恒重,测得固体质量减少了0.42g,剩余固体在580℃时继续加热至恒重,固体质量又减少了0.75g.请通过计算确定该碱石灰各成分的质量分数.
分析:(1)①依据溶液中电荷守恒计算得到;
②依据碱石灰的组成物质结合极值分析判断得到钠离子和钙离子的物质的量的关系;
n (Na+)=x mol、n (Ca2+)=y mol,依据氢氧化钠和氧化钙,氢氧化钠和氢氧化钙混合物的质量结合极值分析得到;
(2)Ca(OH)2在250℃时不分解、NaOH在580℃时不分解,取市售碱石灰4.0g,在250℃时加热至恒重,测得固体质量减少了0.42g,为水;剩余固体在580℃时继续加热至恒重,固体质量又减少了0.75g.为减少的氢氧化钙分解生成的水,计算得到氢氧化钙的质量;剩余固体质量为氢氧化钠质量;
解答:解:(1)①氢氧化钙和氢氧化钠溶液中存在电荷守恒,浓度关系也是微粒物质的量的关系,n(OH-)=2n(Ca2+)+n(Na+),所以得到n(Na+)=n(OH-)-2n(Ca2+);
故答案为:n(OH-)-2n(Ca2+);
②碱石灰是NaOH、CaO,n (Na+)、n (Ca2+)的关系 40x+56y=4;
碱石灰是NaOH、CaO、Ca (OH)2,n (Na+)、n (Ca2+)的关系 40x+56y<4.0<40x+74y
碱石灰是NaOH、Ca (OH)2,n (Na+)、n (Ca2+)的关系 40x+74y=4.0;
碱石灰是NaOH、CaO、Ca (OH)2、H2O,n (Na+)、n (Ca2+)的关系 40x+74y<4.0
故答案为:
可能组成 NaOH、CaO NaOH、CaO、
Ca (OH)2 NaOH、
Ca (OH)2 NaOH、
Ca (OH)2、H2O n (Na+)、n (Ca2+)
的关系 40x+56y=4 40x+56y<4.0<40x+74y 40x+74y=4.0 40x+74y<4.0
(2)Ca(OH)2在250℃时不分解、NaOH在580℃时不分解,取市售碱石灰4.0g,在250℃时加热至恒重,测得固体质量减少了0.42g,说明碱石灰中含有水,质量分数=×100%=10.5%;剩余固体在580℃时继续加热至恒重,固体质量又减少了0.75g.减少的为氢氧化钙分解生成的水,氢氧化钙的质量=×74g/mol;碱石灰中氢氧化钙质量分数=×100%=77.1%;氢氧化钠质量=4.0g-0.42g-3.083g=0.497g,氢氧化钠质量分数=×100%=12.4%;
答:该碱石灰各成分的质量分数:H2O%=10.5%; Ca(OH)2%=77.1%; NaOH%=12.4%;
点评:本题考查了物质组成的探究实验分析判断和计算,掌握物质性质和物质组成的分析方法是解题关键,注意题干条件的分析应用,题目难度中等.
练习册系列答案
相关习题
科目:高中化学来源:题型:
 某同学设计如图装置,研究非金属元素性质变化规律.
某同学设计如图装置,研究非金属元素性质变化规律.
(1)已知硅酸(H2SiO3)是一种难溶于水的弱酸,呈白色.在化学反应中,一般地,强酸能制弱酸,如NaHCO3+HCl═NaCl+CO2↑+H2O,得出:HCl酸性强于H2CO3的酸性.现有硝酸溶液、碳酸钙、澄清石灰水、硅酸钠溶液,选择试剂用如图装置证明:酸性:HNO3>H2CO3>H2SiO3.
A中装试剂
硝酸溶液
硝酸溶液
,B中装试剂
碳酸钙
碳酸钙
,C中装试剂
硅酸钙
硅酸钙
.C中实验现象为
产生白色沉淀
产生白色沉淀
;写出C中发生反应的离子方程式
CO2+SiO32-+H2O=H2SiO3↓+CO32-
CO2+SiO32-+H2O=H2SiO3↓+CO32-
.
(2)已知高锰酸钾在常温下与浓盐酸反应产生氯气,利用如图装置证明氯气氧化性强于碘单质的氧化性.则A中装浓盐酸,B中装入高锰酸钾粉末,C中装试剂
淀粉-KI溶液
淀粉-KI溶液
,C中现象
溶液变蓝色
溶液变蓝色
,写出离子方程式
2I-+Cl2═I2+2Cl-
2I-+Cl2═I2+2Cl-
.该实验装置有明显不足,请指出改进方法:
增加装有氢氧化钠溶液的尾气吸收装置
增加装有氢氧化钠溶液的尾气吸收装置
.
(3)如果C中装饱和氢硫酸溶液,A中装浓盐酸,B中装高锰酸钾溶液,反应开始后观察现象是C中产生淡黄色沉淀,写出化学方程式
Cl2+H2S═S↓+2HCl
Cl2+H2S═S↓+2HCl
;证明氯的非金属性比硫的非金属性
强
强
(填“强”或“弱”或“无法判断”).
查看答案和解析>>
科目:高中化学来源:题型:
(2009?松江区二模)在氢氧化钠浓溶液中加入氧化钙,加热制成的白色固体就是碱石灰.已知:氢氧化钙在250℃时开始分解,氢氧化钠在580℃时不分解.取市售碱石灰4.000g,在450℃时加热至恒重,测得固体质量减少了0.360g,把剩余固体完全溶于水,加入足量的Na2CO3溶液,得到5.000克沉淀.求:
(1)该碱石灰中钙元素的质量分数
50%
50%
;
(2)该碱石灰中各成分的物质的量
NaOH:0.021mol,Ca(OH)2:0.02mol,CaO:0.03mol
NaOH:0.021mol,Ca(OH)2:0.02mol,CaO:0.03mol
.
查看答案和解析>>
科目:高中化学来源:题型:
用图1-3所示装置(酒精灯、铁架台等未画出)制取三氯化磷。在具支烧瓶d中放入足量白磷,将氯气迅速而又不间断地通入具支烧瓶中,氯气与白磷就会发生反应,产生火焰。三氯化磷和五氯化磷的物理常数见下表。
熔点/℃
沸点/℃
三氯化磷
-122
76
五氯化磷
148
200 ℃分解
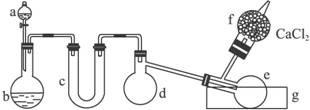
图1-3
(1)有浓盐酸、浓硫酸、白磷、二氧化锰、氢氧化钠等物质供选用,a、b中应该装入的试剂分别是:a________,b________。
(2)________(填仪器对应的字母)仪器需要加热。
(3)生成的三氯化磷在蒸馏烧瓶e中收集。为保证三氯化磷蒸气冷凝,应在水槽g中加入________。
(4)三氯化磷遇到水蒸气强烈反应,甚至发生爆炸,所以d、e仪器及装入其中的物质都不能含有水分。为除去氯气中的水分,c可以装入下列物质中的________(填字母)。
A.碱石灰 B.浓硫酸 C.无水氯化钙
(5)氯气和白磷反应放出大量的热,为使具支烧瓶d不致因局部过热而炸裂,实验开始前应在烧瓶的底部放少量________。
(6)实验室的白磷保存于水中,取出白磷后用滤纸吸干表面水分,浸入无水酒精中片刻,再浸入乙醚中片刻即可完全除去水分。已知水与酒精互溶,酒精与乙醚互溶,用上述方法可除去水的原因是________________________________________________________。
(7)为防止氯气污染空气,装置末端导出的气体最好用(填字母)________进行净化处理。
A.NaOH溶液 B.Ca(OH)2溶液 C.饱和食盐水
查看答案和解析>>
科目:高中化学来源:题型:
用图1-3所示装置(酒精灯、铁架台等未画出)制取三氯化磷。在具支烧瓶d中放入足量白磷,将氯气迅速而又不间断地通入具支烧瓶中,氯气与白磷就会发生反应,产生火焰。三氯化磷和五氯化磷的物理常数见下表。
熔点/℃
沸点/℃
三氯化磷
-122
76
五氯化磷
148
200 ℃分解
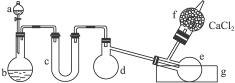
图1-3
(1)有浓盐酸、浓硫酸、白磷、二氧化锰、氢氧化钠等物质供选用,a、b中应该装入的试剂分别是:a________,b________。
(2)________(填仪器对应的字母)仪器需要加热。
(3)生成的三氯化磷在蒸馏烧瓶e中收集。为保证三氯化磷蒸气冷凝,应在水槽g中加入________。
(4)三氯化磷遇到水蒸气强烈反应,甚至发生爆炸,所以d、e仪器及装入其中的物质都不能含有水分。为除去氯气中的水分,c可以装入下列物质中的________(填字母)。
A.碱石灰 B.浓硫酸 C.无水氯化钙
(5)氯气和白磷反应放出大量的热,为使具支烧瓶d不致因局部过热而炸裂,实验开始前应在烧瓶的底部放少量________。
(6)实验室的白磷保存于水中,取出白磷后用滤纸吸干表面水分,浸入无水酒精中片刻,再浸入乙醚中片刻即可完全除去水分。已知水与酒精互溶,酒精与乙醚互溶,用上述方法可除去水的原因是________________________________________________________。
(7)为防止氯气污染空气,装置末端导出的气体最好用(填字母)________进行净化处理。
A.NaOH溶液 B.Ca(OH)2溶液 C.饱和食盐水
查看答案和解析>>
科目:高中化学来源:2009年上海市松江区高考化学二模试卷(解析版)题型:解答题
在氢氧化钠浓溶液中加入氧化钙,加热制成的白色固体就是碱石灰.已知:氢氧化钙在250℃时开始分解,氢氧化钠在580℃时不分解.取市售碱石灰4.000g,在450℃时加热至恒重,测得固体质量减少了0.360g,把剩余固体完全溶于水,加入足量的Na2CO3溶液,得到5.000克沉淀.求:
(1)该碱石灰中钙元素的质量分数______;
(2)该碱石灰中各成分的物质的量______.
查看答案和解析>>
网址:已知:在氢氧化钠浓溶液中加入氧化钙.加热.制成的白色固体就是碱石灰.有两个实验小组的同学决定通过实验探究碱石灰的组成.(1)第一小组设计方案的流程如下:①写出n (OH https://www.yuejiaxmz.com/news/view/65241
相关内容
下列各组物质能在pH=1的无色溶液中大量共存的是( ) A.K2SO4漂白粉在社会生活.工业生产中用途广泛.它除了具有漂白作用外.还能杀菌消毒.(1)漂白粉的主要成分为CaCl2.Ca(ClO)2.工业上制取漂白粉的反应为2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O.(2)漂白粉长期暴露在空气中会逐渐失效.写出该过程中发生的化学方程式Ca(ClO)2+CO2+H2O=CaCO3+2HClO.2HCl 题目和参考答案——青夏教育精英家教网——
100个在家就能做的化学小实验 简单的化学趣味小实验大全
以下是我们日常生活中常用各种清洗剂.选择适当的用品可以得到更好的清洗效果.名称洗涤灵洁厕灵炉具清洁剂污渍爆炸盐漂白粉产品样式有效成分或功能清洗油污盐酸氢氧化钠过碳酸钠消毒(1)我们使用洗涤灵清洗餐具上的油污.这是因为它具有 的功能.(2)以下物质可以使用洁厕灵清洗的是 填字母序号).a.铁锈 b.油渍 c.水垢(主要成分为碳酸钙和氢氧化镁)(3) 题目和参考答案——青夏教育精英家教网——
金属在日常生活中应用广泛.(1)用锌片和硫酸铜溶液的反应可呈现“铁树开花 的美景.该反应的化学方程式是 .(2)铁制品在喷漆前需放入稀盐酸中除锈.除铁锈的化学方程式是 . Zn + CuSO4 === ZnSO4 + Cu Fe2O3 + 6HCl === 2FeCl3 + 3H2O [解析] (1)锌和硫酸铜反应生成硫酸锌和铜.反应的化学方程式是Zn + 题目和参考答案——青夏教育精英家教网——
已知生活中厕所清洁剂的pH=1,厨房的清洁剂的pH=12。下列关于两者的说法错误的是( )
如图是三种日常生活中常用的化工产品.请回答下列问题:的有效成分为过氧化氢.长期存放会失效.用化学方程式解释失效的原因2H2O2=2H2O+O2↑.含有盐酸.与“84 消毒液(图3)混合会发生如下反应:2HCl+NaClO═X+H2O+Cl2↑.对人体造成伤害.下列说法正确的是ABC.A.X的化学式为NaCl B.对人体造成伤害的物质是氯 题目和参考答案——青夏教育精英家教网——
下列是生活中常见物质的pH,其中碱性最强的是( )A.厕所清洁剂pH=1
小苏打在日常生活中有广泛的用途.工业上制取小苏打有多种方法.其中有一种是气相固碳法.其利用的原理是:Na2CO3+H2O+CO2=2NaHCO3资料1:NaHCO3+NaOH=Na2CO3+H2O资料2:碳酸钠和碳酸氢钠的溶解度表温度/℃0152030405060碳酸氢钠溶解度/g6.98.729.611.112.714.4516.4碳酸钠溶解度/g7.713.2521.839.74 题目和参考答案——青夏教育精英家教网——
碱性最强的是( )A. 牙膏pH=9 B. 食盐水pH=7 C. 白醋pH=3 D. 洗洁精pH=11 D [解析]白醋的pH=3.显酸性,食盐水pH=7.显中性,洗洁精.牙膏等物质的pH大于7.显碱性.洗洁精的pH最大.碱性最强.故选D. 题目和参考答案——青夏教育精英家教网——

