29.碳及其含碳化合物在人们的生产生活中应用广泛. (1)天然气是人们日常生活中的清洁能源. 已知①CH4(g)+2O2(g)=CO2(g)+2 H2O(l), △H1=
人工智能在日常生活中的应用越来越广泛 #生活常识# #科技日新月异#
29.(15分)碳及其含碳化合物在人们的生产生活中应用广泛。
(1)天然气是人们日常生活中的清洁能源。
已知①CH4(g)+2O2(g)=CO2(g)+2 H2O(l); △H1=-890.3kJ·mol-1
②2 CO(g)+O2(g)=2CO2 (g); △H2=-566 kJ·mol-1
则反应2 CH4(g)+3O2(g)=2CO(g)+4H2O(l)的△H=_____________。
(2)甲烷燃料电池的化学方程式为CH4+2O2=CO2+2H2O。某甲烷燃料电池以甲烷为燃料,以空气为氧化剂,以熔融的K2CO3(其中不含O2-和)为电解质,以具有催化作用和导电性能的稀土金属为电极。
该燃料电池的负极电极反应式为:CH4-8e-+4=5CO2+2H2O,则其正极电极反应式为____________;为使电解质的组成保持稳定,使该燃料电池长时间稳定运行,在通入的空气中必须加入________________物质。
(3)以该燃料电池为电源,以铂作电极电解1000g 4.55%的NaOH溶液,一段时间后,溶液中溶质的质量分数变为5.00%,则阳极产生的气体在标准状况下的体积为________L。
(4)将不同量的CO(g)和H2O(g)分别通入到体积为2 L的恒容密闭容器中,进行反应CO(g)+H2O(g)CO2(g)+H2(g),得到如下三组数据:
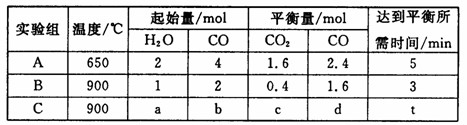
①实验A中以v(H2)表示的反应速率为___________________。
②通过计算可知,CO的转化率实验A_______________实验B(填“大于”、“等于”或“小于”),该反应的正反应为______________热反应(填“吸”或“放”)。
③若实验C要达到与实验B相同的平衡状态,则a、b应满足的关系是_________________(用含a、b的数学式表示)。
网址:29.碳及其含碳化合物在人们的生产生活中应用广泛. (1)天然气是人们日常生活中的清洁能源. 已知①CH4(g)+2O2(g)=CO2(g)+2 H2O(l), △H1= https://www.yuejiaxmz.com/news/view/219744
相关内容
随着环保意识增强.清洁能源越来越受到人们关注.(1)甲烷是一种理想的洁净燃料.已知:CH4(g)+2O2(g)═CO2(g)+2H2O(g),△H=(1)甲烷是一种高效清洁的新能源.0.25mol甲烷完全燃烧生成液态水时.放出222.5kJ热量.则甲烷燃烧热的热化学方为CH4(g)+2O2(g)→CO2(g)+2H2O(l)△H=
日常生活、生产中甲烷既是重要的清洁能源也是一种重要的化工原料.(1)如图1是CH4/H2O体系放氢焓变示意图:则CH4(g)+CO2(g)=2CO(g)+2H2(g)△H=
甲醇是人们开发和利用的一种新能源.已知:①2H2(g)+O2(g)═2H2O(l)△H1=
丙烯是重要的有机化工原料,丁烯催化裂解法是一种重要的丙烯生产法,生产过程中会有生成乙烯的副反应发生。反应如下:I主反应,3C4H8(g)=4C3H6(g)△H1
利用CO2和CH4重整可制合成气(主要成分为CO.H2).已知重整过程中部分反应的热化学方程式为:①CH4+2H2(g)△H=+75.0KJ•mol
(8分)甲醇是人们开发和利用的一种新能源。已知:①2H2(g)+O2(g)===2H2O(l)ΔH1=-571.8kJ/mol;②CH3OH(g)+1/2O2(g)===CO2(g)+2H2(g)ΔH2=-192.9kJ/mol。(1)甲醇蒸气完全燃烧的热
甲醇是一种可再生能源,具有广泛的开发和应用前景.(1)工业上一般采用下列两种反应合成甲醇:反应I:CO(g)+2H2(g)CH3OH(g)ΔH1反应II:CO2(g)+3H2(g)CH3OH(g)+H2O(g)ΔH2①上述反应
在36g碳不完全燃烧所得气体中,CO占体积1/3,CO2占体积2/3,且C(s)+1/2O2(g)=CO(g)△H=-110.5kJ/molCO(g)+1/2O2(g)=CO2(g)△H=-283kJ/mol与这些碳完全燃烧相比,损失的热量是
消除含氮化合物对大气和水体的污染是环境保护的重要研究课题。(1)已知:反应ⅠN2(g)+O2(g)=2NO(g)ΔH=akJ·mol-1反应Ⅱ2NO(g)+O2

