【论肿道麻】Nature Communications: 昼夜节律对衰老和长寿的重要性
避免长时间熬夜,规律作息对身体抗衰老至关重要 #生活技巧# #健康生活方式# #抗衰老#

饮食限制(DR)可以减轻体重、改善健康和延长寿命。通过控制食物供应量和/或时间,以及调整营养成分可实现DR。由于这些因素通常在DR期间结合在一起,尚不清楚哪些是有益效果所必需的。许多靶向营养敏感基因通路的药物在一天中的表达有变化,表明给药时机至关重要。2021年5月德克萨斯大学西南医学中心的研究人员于《Nature Communications》杂志发表了一篇名为“Importance of circadian timing for aging and longevity”的综述,作者对饮食和药物干预如何通过影响能量摄入和昼夜节律促进健康寿命进行了讨论。

衰老是慢性病(包括肥胖、糖尿病、癌症、心血管疾病和神经退行性疾病)的主要危险因素。目前,老龄化研究的重点是缩短寿命与健康寿命之间的差距。健康寿命的生物标记物包括:代谢物(葡萄糖、胆固醇、脂肪酸)水平、生物学过程(炎症、自噬、衰老、血压)和生物学功能(行为、认知、心血管表现、健康和虚弱)。动物研究表明,衰老过程可通过遗传基因、营养和药理学干预来实现。
饮食限制可以广泛地提高寿命和健康水平,可能通过昼夜节律系统介导。本文回顾了动物模型和人体试验的文献,评估了喂养模式和食物质量对昼夜节律、健康和寿命的影响。最后,讨论了昼夜节律医学的概念,认为这是制定抗衰老措施的一个机会。
昼夜节律与衰老
哺乳动物中,昼夜节律系统控制每日(约24小时)的行为和生理节律。位于下丘脑视上核(SCN)的中央生物钟通过体液和神经信号同步全身组织中的外周生物钟。葡萄糖、脂肪酸和胆固醇代谢通路受昼夜节律控制,生物钟基因的破坏会使健康状况恶化。此外,由于与中央生物钟基因的直接串扰,与衰老相关的营养敏感通路的组件表现出组织特异性振荡(图1-2)。

图1.昼夜节律生物钟、营养敏感和代谢通路的分子组成之间的串扰
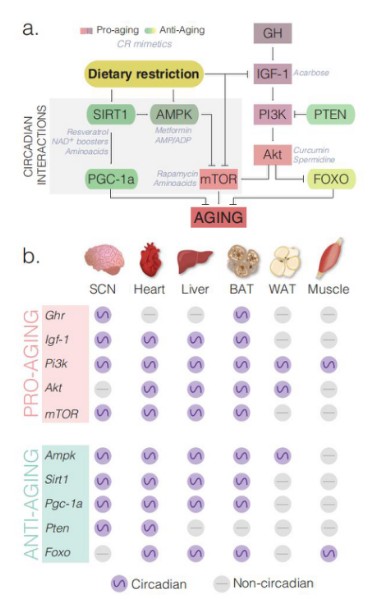
图2.受饮食干预调节的衰老相关通路呈昼夜节律振荡
内分泌系统也受昼夜节律调节。人类胰岛素、生长激素释放肽、脂联素和皮质醇在上/下午升高,而褪黑素、促甲状腺素、泌乳素、瘦素、生长激素(GH)和成纤维细胞生长因子21(FGF-21)在夜间升高。这些激素调节进食和睡眠,并同步内源性生物钟。
昼夜节律的系统性影响与衰老直接相关。高振幅的昼夜节律有利于健康和延长寿命,而随着正常衰老,昼夜节律的振幅降低,常表现出相移。此外,老龄动物在光/暗周期的周期转换/同步性方面存在缺陷,损害了生物体预测和适应环境变化的能力。
内部生物钟和环境变化不匹配对生存有害。生物钟基因有缺陷的啮齿类寿命短。而使昼夜节律恢复正常的措施可以改善寿命。衰老如何干扰内部生物钟功能是一个悬而未决的问题,但了解生理和代谢的昼夜节律调节可能为设计和实施抗衰老措施提供新见解。
动物模型中的喂养模式
除了热量成分,喂食时间和禁食时间也会影响健康。昼夜节律系统与代谢、表观遗传特征和年龄相关疾病之间的联系机制仍有待阐明。此外,外周生物钟在衰老过程中调节代谢稳态的作用尚不清楚。理解饮食干预中昼夜节律调节之间的机制联系,可能会为我们提供如何在一生中实现最佳健康益处的见解。本文讨论了动物模型中最常用的DR范式:热量限制(CR)、时间限制(TR)和间歇性禁食(IF)及饮食成分的变化对健康和寿命的影响(图3)。

图3.饮食干预可预防慢性病并延长寿命
热量限制(CR)
CR可延长寿命,改善组织健康。CR改善了衰老的几个特征,包括对营养敏感通路的调控放松、线粒体功能障碍、自噬受损、干细胞衰老、DNA损伤和炎症。
CR通过靶向高度保守的通路延长寿命。包括抑制IGF-1和mTOR,以及激活SIRT1、NAMPT、AMPK、FGF-21和PGC-1α信号通路(图2a)。这些分子表现出组织特异性昼夜节律振荡(图2b和补充表1),其中一些反馈到生物钟的分子成分(图1)。
抑制胰岛素/IGF-1信号通路延长了从线虫到小鼠的寿命。IGF-1水平随正常和过早衰老而下降,可能是对能量不足的防御反应。IGF-1在小鼠组织中的表达振荡。此外,在缺乏核心时钟基因(Cry1/2-/-)小鼠中,肝脏和血液中的IGF-1节律被消除。IGF-1的下游靶点也显示出组织特异性振荡,表明全身的IGF-1信号处于昼夜节律控制之下。IGF-1可能是使外周生物钟与喂食时间同步的信号之一;然而,IGF-1通路在整个生命周期中的昼夜调节在很大程度上未被探索。
mTOR在能量代谢中起关键作用,并调节苍蝇和小鼠的昼夜节律。CR可能通过进食/禁食周期,恢复小鼠即食喂养时丢失的mTOR节律性活动。此外,禁食时核心时钟蛋白PER2的诱导驱动mTOR抑制。这表明,内源性生物钟和CR均调节mTOR的节律活动。
衰老过程对核心时钟机制影响最小,反而促进转录组的组织特异性重排。有趣的是,BMAL1缺陷小鼠不仅寿命缩短,还表现出早衰表型。令人惊讶的是,CR降低了Bmal1−/−小鼠的存活率,但未降低IGF-1和胰岛素水平或改善生物钟基因的昼夜节律。目前尚不清楚这是否是BMAL1的特异性作用,或CR是否对其他生物钟突变小鼠也有不利影响。
对CR的组织特异性反应增加了理解营养敏感通路对寿命的相对贡献的复杂性。例如,有人提出激活SIRT1来调节CR对寿命的影响。然而,尽管CR增加了大多数组织中的SIRT1,但却降低了肝脏中的SIRT1。此外,虽然SIRT1的脑特异性表达足以延长小鼠寿命,但全身SIRT1的过表达没有这种益处。因此,关于CR对不同组织的有益作用,仍存在许多问题,其中组织特异性昼夜节律可能起重要作用(图2和补充表1)。
CR方案通常受人日程安排限制,早晨提供食物。由于获得食物的机会有限,啮齿动物往往会在有食物时就吃掉,从而强加每天的进食和禁食周期。因为摄入食物会同步全身的代谢功能和激素产生,所以进食时机至关重要。一项有趣的研究发现,CR的长期影响可能与进食时间无关。食物获取时间本身的影响已成为新的探索领域。
时间限制(TR)
包括食物在内的环境信号可以充当强大的生物钟诱引剂。当将食物接触限制在白天几小时内,啮齿类动物会增加活动。这种TR模式也会在外周生物钟中将昼夜节律的相位改变数小时,而对SCN没有显著影响。然而,TR与CR或食物的结合会产生强大的刺激,能重置中枢和外周生物钟。
小鼠在夜间(活动期)消耗75–85%的热量,而高脂饮食(HFD)在休息期增加约50%的摄入,这种喂食行为扰乱会导致HFD小鼠肥胖和糖尿病的发展。一天中只在错误时间进食会增加体重增长及对肥胖、糖尿病和心血管疾病的易感性,也会对学习和记忆产生负面影响。相反,将食物摄入限制在活动期可防止HFD引起的肥胖、肝脂肪变性、高胰岛素血症和炎症。但TR对寿命的影响有待确定。
禁食
慢性间歇性禁食(IF)包括交替24小时少量食物摄入和24小时无限制摄入,或周期性禁食(PF)几天。在啮齿类动物中,IF延长寿命,可以防止肥胖、心血管疾病、高血压、糖尿病和神经退行性疾病。GH/IGF-1信号似乎是IF效应的关键介质。IF改变了肝脏生物钟基因的相位,但对中枢和外周生物钟的长期影响尚不清楚。
两餐之间的禁食期能延长小鼠寿命。当提供与无限制喂食摄入相当的每日一餐(MF)时,MF小鼠比24小时进食的小鼠活得更长。记录无限制地进食模式作为每只小鼠的基线,将有助于确定强制喂食方案(CR、TR或IF)对其他进食参数的影响程度。因此,需进一步的研究来阐明食物摄入量和时间对存活率的影响。
一种模拟禁食的饮食(FMD)可以提供与长期禁食相似的益处,而不需饥饿。FMD是一种低热量/低蛋白饮食,增强小鼠认知功能,减少肥胖,改善骨质流失,降低肿瘤发生率,增强免疫系统,但不延长最长寿命。FMD恢复1型糖尿病(T1D)患者的胰岛素分泌,并逆转小鼠模型中的T1D和T2D表型。此外,它还会降低循环中IGF-1、胰岛素和葡萄糖水平,同时增加血浆中IGF结合蛋白1和酮体的浓度及原干细胞的数量。因此,这种模拟禁食的方法有效延长了健康期。
改变食物成分
饮食限制依从性往往会随时间推移而降低。作为替代方案,研究探索了减少特定饮食成分,而不减少总体食物摄入量。其中两个例子是生酮饮食(KD)和蛋白质限制(PR)。
KD是一种低碳水化合物、高脂肪饮食。KD可延长小鼠健康寿命,并增加中位寿命,但不延长最长寿命。与HFD不同,KD不会改变进食模式,小鼠主要在夜间进食。这可能会增强组织特异性节律,有助于改善整体健康。
限制饮食中的蛋白质或某些氨基酸也可以降低年龄相关疾病的发病率,延长寿命。在啮齿类动物和人类中,蛋白质限制增加了肝脏因子FGF-21。小鼠FGF-21的过度表达通过抑制肝脏中的GH/IGF-1信号通路来延长寿命。过度表达FGF-21的小鼠具有高度的节律性。除PR外,蛋氨酸限制(MR)可以延长正常衰老和加速衰老小鼠模型的健康和寿命。补充甘氨酸可以模拟MR并延长啮齿类动物的寿命。这些研究表明,限制特定的饮食成分是在不持续CR的情况下改善代谢功能的另一可行选择。进一步研究需确定在一天中的最佳时间限制或补充是否可以扩大其对健康和寿命的益处。
对人类健康的影响
人类的热量限制和模拟禁食饮食
长期CR改善了人类的几种健康标志物,包括体重、代谢率和氧化损伤降低,心血管疾病和癌症的发病率降低,胰岛素-AKT-FOXO信号通路活性降低。
临床试验表明,交替禁食可以减轻体重、改善血脂状况、降低血压和增加胰岛素敏感性。禁食增加癌症患者对某些化疗药的敏感性。此外,HER2阴性II/III期乳腺癌患者化疗期间禁食耐受性良好,血液毒性降低。
KD可以使睡眠模式正常化,减轻体重。在健康、非肥胖、正常的睡眠者中,KD会增加慢波睡眠,减少REM睡眠。低甲硫氨酸饮食也通过增加人体循环中的FGF-21水平而带来代谢益处。
时间限制(TR)
与瘦人相比,非瘦人在更接近褪黑素起效(标志着每个人夜晚的开始)的1.1小时内消耗了大部分热量,表明食物摄入时间也是新陈代谢的关键方面。
限时进食可以降低人体脂肪、空腹血糖及胰岛素水平、胰岛素抵抗、高脂血症和炎症。在一天中较早进食,会有进一步的好处。早吃晚餐改善了葡萄糖耐量,支持了人类昼夜节律性褪黑素和血糖控制之间的联系。
在实验室环境中,人类的分子生物钟可能受进食时间调节,并可能影响血浆葡萄糖。与高热量晚餐相比,健康者在吃高热量早餐时表现出较低的葡萄糖水平,减少饥饿感,并增加饮食诱导的产热。
昼夜节律系统失调的后果
基因多态性使一些人表现为早鸟(早睡型)或夜猫子(晚睡型)。晚睡型可能有害,因为这些人通常会经历轻微的昼夜节律失调。
研究发现,晚睡型与糖尿病患者更高的炎症相关。在时差和轮班工作中,昼夜节律与环境的被迫失调会增加患2型糖尿病和癌症的风险。
在另一项研究中,14名健康瘦削的年轻男性接受了更剧烈的12小时轮班失调方案。结果表明,即使在实验室环境中发生短期昼夜节律失调,人类的糖耐量也可以改变。
睡眠限制
睡眠总时间也会影响新陈代谢和健康。睡眠剥夺导致交感神经系统活动增加,夜间皮质醇升高,白天GH水平升高。限制睡眠后,瘦素水平较低,胃饥饿素水平较高。部分睡眠剥夺后,受试者的能量摄入增加了约385千卡。由于总能量消耗或静息代谢率没有显著变化,睡眠剥夺导致正性能量平衡,可能有助于体重增加。睡眠限制还会延长进食时间,增加对富含能量的零食的偏好。
昼夜节律医学:优化治疗时机
国家老龄干预研究所测试项目(ITP)旨在评估可能延长小鼠寿命、延缓疾病发作和功能障碍的治疗方法。成功的治疗包括FDA批准的治疗癌症和糖尿病的药物,如雷帕霉素(mTOR抑制剂)和二甲双胍(AMPK激活剂)。这些药物被归类为热量限制类似物(CRMs),因为它们在不限制食物摄入的情况下赋予CR的健康益处(图2)。超过80%的FDA批准药物的靶点表现出每日节律。因此,剂量定时可能有助于优化抗衰老药物的益处(图2,4)。
出于实际原因,在小鼠身上测试的大多药物都是夜间给药,可能不是最佳时机,因为这些药物的靶点具有昼夜节律的表达。昼夜节律医学基于以下证据:(1)昼夜节律随年龄增加而减弱,(2)扰乱昼夜节律导致代谢紊乱和寿命缩短,而恢复昼夜节律促进健康和长寿,(3)与衰老相关的通路全天都在振荡。因此,可假设有最佳给药时间,可以恢复目标的适当节律,最终导致寿命延长(图4),而次优给药时间不会有任何益处。因此,有必要开发新的工具,在特定时间实施干预措施,同时控制频率和数量。

图4.昼夜节律医学如何作为改善昼夜节律和潜在促进寿命的优化干预模型
许多治疗衰老相关疾病的例子,如在一天中特定时间服药,会更有效,包括癌症、T2D和高血压。阿司匹林被用作人类心血管疾病(CVD)的二级预防,其有效性和疗效很大程度上取决于给药时机。试验表明,阿司匹林在睡前比在早上服用更有效地减少人类血液凝结。65岁以上的健康老人在早餐期间服用阿司匹林会增加出血、CVD风险和全因死亡率。
多胺强调了药学干预如何介导生物钟、代谢途径和寿命之间的串扰。补充亚精胺和高多胺饮食都能延长啮齿动物的寿命。多胺表现出昼夜节律振荡,并通过调节PER2/CRY1相互作用影响昼夜节律周期。值得注意的是,多胺振荡表现出衰老依赖性周期延长,可以通过饮食中补充多胺来逆转。
其他延缓衰老相关疾病的潜在药物是针对内源性生物钟的。在小鼠中,一种叫川陈皮素(NOB)的天然黄酮类化合物可以在不改变食物摄入、刺激能量消耗和昼夜节律活动的情况下减少体重增加,增强葡萄糖和胰岛素耐受性,降低脂质含量,并改善线粒体呼吸。表明维持生物体内强大的昼夜节律组织可以防止代谢紊乱。
推断个体内部计时的方法
已经开发了几种算法来识别体内时间标记。第一种称为分子时间表,由大约100个从老鼠肝脏芯片数据集中识别出来的时间指示基因组成。大多数组织的全基因组数据集很少包括采集样本的时间,为此开发了一些算法:CYCLOPS能揭示人类转录节律;BodyTime,用于确定人在一天中任何时候从单个血样中采集的内部时间;以及TimeSignature,旨在使用约40个基因来预测从血样(±2h)中采集的内部时间。这些都为转化研究和个体化昼夜节律医学提供了有希望的工具(图4)。
昼夜节律系统对重置信号非常敏感。此外,延长小鼠寿命的药物干预通常表现出性别二态性,并取决于治疗开始的年龄,因此,也是需要考虑的重要因素。
“论肿道麻”述评
随着人口老龄化,慢性病风险增加已成为全球公共卫生负担。饮食干预,包括调节食物摄入数量和时间以及禁食期长短,已成为缓解年龄相关身体衰退和慢性病的方法。展望未来,重要的是阐明热量限制方案的影响归因于热量、禁食和进食时间的程度。此外,靶向经DR改善的通路的药物干预有望成为限制性饮食的替代品。了解代谢通路在一天中如何变化,可能有助于了解何时以及多久治疗一次,以尽量减少耐药性和副作用(图4)。需要进行系统研究,以确定在什么年龄治疗可提供最大益处。将组织特异性昼夜节律振荡整合到这些通路中,对于确定实施干预措施的最佳时间也至关重要。
编译:刘配配;述评:翁梅琳
审校:张军,缪长虹
参考文献:Acosta-Rodríguez VA, Rijo-Ferreira F, Green CB, et al. Importance of circadian timing for aging and longevity. Nat Commun. (2021) 12: 2862. https://doi.org/10.1038/s41467-021-22922-6.
声明:古麻今醉公众号为舒医汇旗下,古麻今醉公众号所发表内容之知识产权为舒医汇及主办方、原作者等相关权利人所有。未经许可,禁止进行转载、摘编、复制、裁切、录制等。经许可授权使用,亦须注明来源。欢迎转发、分享。
本文由“健康号”用户上传、授权发布,以上内容(含文字、图片、视频)不代表健康界立场。“健康号”系信息发布平台,仅提供信息存储服务,如有转载、侵权等任何问题,请联系健康界(jkh@hmkx.cn)处理。
网址:【论肿道麻】Nature Communications: 昼夜节律对衰老和长寿的重要性 https://www.yuejiaxmz.com/news/view/433079
相关内容
Nature :解读生物节律密码,有效抵抗衰老昼夜节律抗衰新纪元:瑞士NyxSeren引领全球保健品行业新潮流
睡眠不足和昼夜节律失调在肥胖中的作用,Nature Reviews Endocrinology
Nature综述:从衰老研究到衰老干预措施
【学术前沿】专家点评 Nature Commun丨李旻典/张志辉合作团队发布限时进食调节肝脏昼夜节…
人类葡萄糖、脂质和能量代谢的昼夜节律调节
Cell metabolism: 昼夜节律和肠道微生物群使宿主对饮食的代谢反应同步
Cell子刊:肠道菌群通过昼夜节律调节身体对压力的反应
“节律生物学”获诺奖的警示:现代生活方式正在打破人类昼夜节律
何时吃,比吃得少更重要!Science论文显示,在适当时间进食可显著延长寿命

